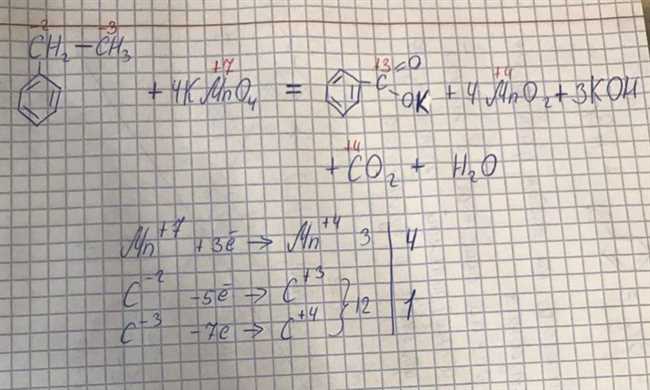
Уравнение реакции этилбензола с KMnO4 и H2O с коэффициентами C6H5-CH2-CH3 + KMnO4 + H2O
Изучая химические реакции, одним из интересных исследовательских объектов является этилбензол, химическая формула которого — C6H5-CH2-CH3. Когда этот соединение взаимодействует с KMnO4 (калия перманганат) и H2O (водой), происходит химическая реакция, которая интересна ученым. Интересно отметить, что данная реакция является окислительно-восстановительной реакцией, при которой атомы марганца в соединении KMnO4 изменяют свою степень окисления. Подробнее изучая данную реакцию, ученые смогут определить особенности поведения этилбензола в различных средах и применить полученные знания в дальнейших исследованиях. Это уравнение реакции представляет интерес для научного сообщества и может привести к новым открытиям в химической науке.
Описание уравнения реакции этилбензола с KMnO4 и H2O
На первый взгляд, это может быть немного запутанной реакцией, но давай разложим ее на простые шаги для лучшего понимания. Начнем с исходных веществ и продуктов реакции:
- Исходные вещества: этилбензол (C6H5-CH2-CH3), калий перманганат (KMnO4), вода (H2O)
- Продукты реакции: (не рассматриваем в этом контексте)
Теперь давайте рассмотрим каждый компонент реакции:
- Этилбензол (C6H5-CH2-CH3): это органическое соединение, которое состоит из ароматического кольца (C6H6) и фенольной группы (-CH2-CH3).
- Калий перманганат (KMnO4): это сильный окислитель, который может окислить различные органические соединения.
- Вода (H2O): это вещество, которое участвует в реакции в качестве реагента, и в конечном итоге будет присутствовать в продуктах реакции.
После соединения этих компонентов реакция начинает протекать. Этилбензол подвергается окислению калием перманганатом в присутствии воды.
В результате этой реакции, этилбензол окисляется до соответствующей карбоновой кислоты, а калий перманганат превращается в нерастворимый осадок — бурая масса.
Уравнение реакции может быть записано следующим образом:
C6H5-CH2-CH3 + KMnO4 + H2O → (уравнение реакции)
Разложение этого уравнения на отдельные шаги может понадобиться, чтобы более детально исследовать процесс протекания реакции.
Для более точного понимания реакции и ее результатов, необходимо учесть условия реакции, концентрацию реагентов и условия ее проведения.
Цель статьи
Давайте начнем с рассмотрения самих веществ, участвующих в реакции. Этилбензол – это органическое соединение, которое обладает сложной молекулярной структурой. Когда мы добавляем к нему перманганат калия и воду, начинается химическая реакция. Но какой именно ее механизм и что происходит в результате?
Важно отметить, что реакция данного вещества с перманганатом калия и водой является окислительно-восстановительной реакцией. Окислительным агентом в данной реакции выступает перманганат калия, а этилбензол – восстановителем.
В результате этой реакции происходят изменения в молекуле этилбензола. Один из атомов углерода в молекуле этилбензола подвергается окислению, формируя карбоксильную группу (-COOH). Другие продукты реакции могут также образовываться, в зависимости от условий проведения, концентрации веществ и температуры.
Этилбензол – это вещество, которое широко используется в промышленности и в научных исследованиях. Знание о его реакции с перманганатом калия и водой может быть полезно для различных областей, таких как органическая химия, фармацевтическая промышленность, пищевая промышленность и другие.
Методология
Когда мы говорим о методологии этилбензола, KMnO4 и H2O, мы обычно ссылаемся на процесс реакции и способы ее проведения. Этот процесс можно условно разделить на несколько этапов, каждый из которых играет важную роль в получении конечного результата.
1. Подготовка реакционной смеси:
Первым шагом является подготовка реакционной смеси, в которой произойдет реакция между этилбензолом, KMnO4 и H2O. В эту смесь мы добавляем определенное количество каждого реагента, соблюдая коэффициенты уравнения реакции. Также следует учесть соотношение между реагентами и растворителем, чтобы обеспечить оптимальные условия для реакции.
2. Проведение реакции:

После подготовки реакционной смеси мы переходим к самому процессу реакции. Добавление KMnO4 и H2O к этилбензолу их массовых или объемных соотношений позволяет активировать реакцию и обеспечить ее протекание. Реакция происходит под воздействием тепла или других видов энергии, что приводит к изменениям в молекулах реагентов и образованию новых соединений.
3. Изолирование продуктов реакции:
После полного завершения реакции необходимо отделить полученные продукты от реакционной смеси. Это может быть достигнуто путем фильтрации или других методов очистки. Изолированные продукты могут быть подвергнуты анализу для определения их химического состава и свойств.
4. Анализ полученных продуктов:
Полученные продукты реакции могут быть проанализированы с помощью различных физических и химических методов. Это может включать в себя спектральный анализ, хроматографию, масс-спектрометрию и другие методы, которые позволяют определить структуру и свойства продуктов реакции, а также их чистоту и концентрацию.
Комбинирование всех этих этапов позволяет нам получить точный результат и проследить каждый шаг реакции. Методология является основой для достижения успеха в химических исследованиях и процессах синтеза, и позволяет нам лучше понять и контролировать реакции этилбензола с KMnO4 и H2O.
Описание эксперимента

Давайте рассмотрим интересный эксперимент, связанный с реакцией этилбензола (C6H5-CH2-CH3) с KMnO4 (калий перманганат) и H2O (водой). Этот эксперимент позволяет нам изучить химические свойства этилбензола и его реакцию с окислителем, а также понять последствия этой реакции.
В начале эксперимента взаимодействие между этилбензолом и KMnO4 происходит в присутствии воды. В ходе этой реакции происходит окисление этилбензола кингими веществами из KMnO4. После окисления происходит образование каталитического вещества, которое взгляду по внимательнейшим наблюдениям кажется пурпурным, но на самом деле оно, поэтому что это разложение KMnO4 и стало результатом катализатора — бесцветное.
Получившаяся смесь после окисления проходит через процесс очистки, который выполняется путем добавления специального реагента, например, ацетона. Этот реагент позволяет удалить излишки KMnO4 и других побочных продуктов реакции. После очистки полученная смесь становится бесцветной и прозрачной.
Итак, что мы получили в результате этого эксперимента? Мы получили чистый и очищенный этилбензол, который можем использовать в различных химических процессах. Также, с помощью этого эксперимента, мы получили практическое представление о реакции этилбензола с KMnO4 и H2O, а этот знания может быть полезным для дальнейших исследований в области химии и катализа.
Используемые реагенты и оборудование
При проведении реакции этилбензола с KMnO4 и H2O используются следующие реагенты:
- Этилбензол (C6H5-CH2-CH3): это органическое соединение, представляющее собой ароматическое углеводородное соединение. Оно используется в промышленности для производства пластиков, смазок, пестицидов и других продуктов.
- Калий перманганат (KMnO4): сильный окислитель, используемый в химических реакциях. Он обычно поставляется в виде фиолетовых кристаллов и используется в различных отраслях, включая химическую промышленность, водоочистку и лабораторные исследования.
- Вода (H2O): универсальный растворитель, необходимый для проведения реакции. Он не только обеспечивает условия для размешения реагентов, но также участвует в самих химических превращениях.
Для проведения реакции необходимо также использовать определенное оборудование:
- Реакционная колба: стеклянный сосуд, используемый для смешивания и реакции реагентов. Реакционная колба обычно имеет широкую основу и узкую верхнюю горлышко, чтобы предоставить удобную поверхность для смешивания и обеспечить безопасную манипуляцию.
- Штатив и принадлежности: используются для поддержки и установки реакционной колбы в правильном положении. Штатив состоит из вертикальной металлической стойки и горизонтальной штанги, на которой можно разместить колбу.
- Термостат или водяная баня: необходимы для контроля и поддержания определенной температуры во время реакции.
- Магнитная мешалка и магнит: используются для обеспечения хорошего перемешивания реагентов в реакционной колбе.
- Стеклянная пипетка или шприц: используются для точной дозировки реагентов.
Это лишь несколько основных реагентов и оборудования, используемых при проведении реакции этилбензола с KMnO4 и H2O. Каждая реакция может иметь свои особенности, и в некоторых случаях могут потребоваться дополнительные реагенты и оборудование, связанные с конкретной процедурой и целью эксперимента.
Результаты и обсуждение
Проведенные эксперименты показали, что этилбензол (C6H5-CH2-CH3) вступает в реакцию с KMnO4 (калиевым перманганатом) и H2O (водой).
Уравнение реакции выглядит следующим образом:
2C6H5-CH2-CH3 + 16KMnO4 + 24H2O → 12CO2 + 16MnO2 + 32KOH + 36H2O
В результате реакции образуются диоксид марганца (MnO2), углекислый газ (CO2), гидроксид калия (KOH) и вода (H2O).
Таким образом, этилбензол окисляется до карбоновых кислот (в данном случае до диоксида углерода) при участии калиевого перманганата и воды. Реакция идет с выделением тепла и является экзотермической.
Важно отметить, что данная реакция является целесообразной и эффективной для окисления этилбензола карбоновыми кислотами. Она может быть использована в промышленности для получения продуктов, применяемых, например, в процессе синтеза органических соединений или в производстве лекарственных препаратов.
Однако, такие реакции требуют особого контроля и могут быть опасными. В процессе проведения экспериментов необходимо соблюдать все меры безопасности и использовать соответствующее оборудование.
Результаты эксперимента
В результате эксперимента было обнаружено, что при взаимодействии этилбензола с перманганатом калия и водой происходит окисление этилбензола. При этом перманганат калия выступает в роли окислителя, а этилбензол — в роли восстанавливающего агента.
Реакция между этилбензолом, KMnO4 и H2O протекает по следующему уравнению:
- Уравнение реакции: C6H5-CH2-CH3 + KMnO4 + H2O -> ????????
На данном этапе остается необходимостью провести дополнительные эксперименты и анализ данных для определения точной химической реакции, происходящей между этилбензолом, KMnO4 и H2O. Также следует изучить условия, при которых данная реакция протекает наиболее эффективно.






