- Высшие оксиды: что это такое, где они увеличиваются и кто является их представителями
- Высшие оксиды: что это такое, где они увеличиваются и кто является их представителями
- Определение высших оксидов
- Какие элементы образуют высшие оксиды?
- Где образуются высшие оксиды?
- Каковы свойства высших оксидов?
- Высшие оксиды: что это такое, где они увеличиваются и кто является их представителями
- Места увеличения высших оксидов
- Раздел 3
- Представители высших оксидов
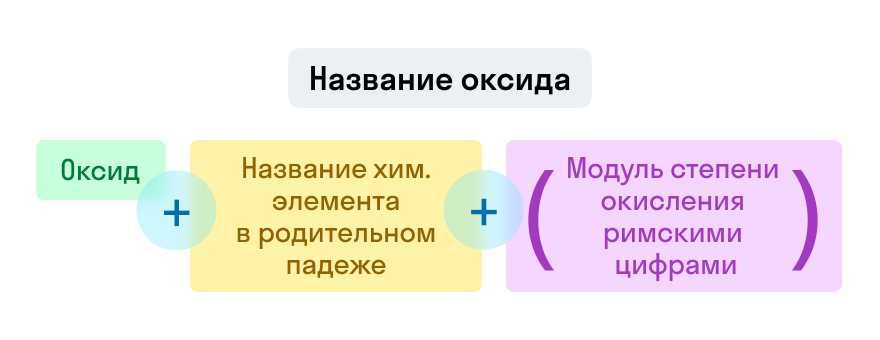
Высшие оксиды – это химические соединения, состоящие из элемента с максимальным возможным оксидационным числом. Они обладают высокой активностью и часто используются в различных промышленных процессах. Главным образом, высшие оксиды увеличиваются у переходных металлов, таких как марганец, хром, железо и другие. Каждый из этих элементов имеет несколько видов высших оксидов, которые отличаются степенью окисления. Например, в марганце существуют МнO, МнО2 и МнO4. Кроме переходных металлов, высшие оксиды также присутствуют у некоторых неметаллов, например, у хлора, серы и фосфора. Знание о высших оксидах не только является важным в химии, но также имеет значительное практическое применение в различных отраслях промышленности, фармацевтике и энергетике.
Высшие оксиды: что это такое, где они увеличиваются и кто является их представителями
Но что же такое высшие оксиды? Это соединения, в которых элемент образует соединение с максимальным окислением. Например, вода (H2O) является оксидом водорода с окислением +1, а пероксид водорода (H2O2) является высшим оксидом водорода с окислением +2.
Наиболее известным и широко используемым представителем высших оксидов является кислород (O2). Кислород — основной компонент воздуха, и его применение в медицине, промышленности и даже в повседневной жизни не подлежит сомнению.
Но кислород далеко не единственный высший оксид. Другими примерами могут быть пероксиды, такие как пероксид бария (BaO2), использование которого в пиротехнике дает яркий кислородно-бариевый огонь, или пероксид натрия (Na2O2), который применяется в качестве отбеливателя и антисептика.
Интересно, что некоторые высшие оксиды имеют важные энергетические свойства. Например, диоксид углерода (CO2) является одним из главных газов, способствующих эффекту парникового газа, и его изучение и управление стали предметом активных научных исследований и политических дискуссий.
Также стоит отметить, что некоторые высшие оксиды обладают электрохимическими свойствами, которые высоко ценятся в различных приложениях. Например, пероксид водорода (H2O2) является одним из наиболее распространенных оксидов в качестве окислителей и антисептиков в медицине и бытовой химии.
Высшие оксиды: что это такое, где они увеличиваются и кто является их представителями
Одним из ярких представителей высших оксидов является озон (O3), который является аллотропной формой кислорода. Он образуется в земной атмосфере при ультрафиолетовом облучении кислорода и играет важную роль в защите от солнечного излучения. Озон используется также в качестве окислителя в промышленных процессах и для очистки воды и воздуха.
Еще одним представителем высших оксидов является пероксид водорода (H2O2), известный как перекись водорода. Он широко используется в медицинских, косметических и бытовых целях, а также в промышленности как окислительное вещество и отбеливатель.
Кроме того, высшие оксиды встречаются в виде молекулярных кислородных соединений, таких как диоксид азота (NO2) и триоксид азота (N2O3). Диоксид азота является одним из основных загрязнителей атмосферного воздуха и может вызывать проблемы с дыханием и здоровьем. Триоксид азота играет роль в образовании кислотного дождя и является важным компонентом атмосферного озона.
Высшие оксиды могут образовываться в различных природных и антропогенных процессах. Например, их увеличение в атмосфере может быть связано с промышленными выбросами, автомобильным транспортом, сжиганием топлива и другими источниками загрязнения воздуха.
Итак, высшие оксиды – это мощные окислители, способные воздействовать на окружающую среду и оказывать как положительное, так и отрицательное воздействие на человека и природу. Знание о них позволяет более осознанно использовать их в промышленности и контролировать их влияние на окружающую среду.
Определение высших оксидов
Какие элементы образуют высшие оксиды?
Высшие оксиды образуются практически из всех химических элементов, но наиболее часто они образуются из переходных металлов, таких как медь, железо, хром и другие. Также высшие оксиды могут быть образованы неметаллами, такими как сера, фосфор и даже углерод.
Где образуются высшие оксиды?
Высшие оксиды могут образовываться в различных средах, таких как воздух, вода, почва и даже организмы живых существ. Например, некоторые известные высшие оксиды, такие как перекись водорода и перекись бария, образуются в атмосфере. Другие высшие оксиды, такие как пероксид натрия и пероксид кальция, могут образовываться водой или в организмах животных и растений.
Каковы свойства высших оксидов?
У высших оксидов есть несколько общих свойств. Во-первых, они обычно являются сильными окислителями, то есть способны передавать электроны другим веществам. Это свойство делает их полезными в различных реакциях окисления.
Во-вторых, высшие оксиды обычно нестабильны и могут разлагаться с выделением кислорода. Например, перекись водорода разлагается на воду и кислород. Это свойство делает их полезными в качестве источников кислорода в различных процессах.
Некоторые высшие оксиды могут также иметь яркую окраску, что делает их полезными в качестве пигментов или красителей. Например, пероксид бария имеет ярко-зеленую окраску и может использоваться при производстве пиротехнических изделий.
Высшие оксиды представляют собой сложные соединения, содержащие большое количество атомов кислорода. Они образуются из различных элементов и могут образовываться в различных средах. Они обладают свойствами сильных окислителей и нестабильны. Высшие оксиды могут использоваться в различных областях, таких как химическая промышленность, медицина и пиротехника.
Высшие оксиды: что это такое, где они увеличиваются и кто является их представителями
Высшие оксиды — это оксиды, в которых элемент имеет наибольшую степень окисления. Это значит, что в молекуле оксида атом элемента соединения имеет максимальное число электронов, которые он может получить или отдать. Этот элемент обычно имеет положительный формальный заряд.
Теперь давайте поговорим о местах, где высшие оксиды увеличиваются. Они обычно возникают в условиях, когда элемент находится в высоком окислительном состоянии или когда он взаимодействует с элементами, имеющими более низкую степень окисления. Например, в присутствии кислорода, многие элементы могут образовывать высшие оксиды. Также высший оксид может образоваться, если элемент взаимодействует с мощным окислителем, таким как луги или сильные кислоты.
Теперь пришло время познакомиться с некоторыми представителями класса высших оксидов. Приведу несколько примеров:
- Марганец (Mn) может образовывать высший оксид — марганцевый диоксид (MnO2).
- Кобальт (Co) образует пероксид кобальта (CoO2), который является высшим оксидом.
- Хром (Cr) может образовать хромовую кислоту (CrO5), также являющуюся высшим оксидом.
| Элемент | Высший оксид |
|---|---|
| Марганец (Mn) | Марганцевый диоксид (MnO2) |
| Кобальт (Co) | Пероксид кобальта (CoO2) |
| Хром (Cr) | Хромовая кислота (CrO5) |
Таким образом, высшие оксиды представляют собой интересные соединения, которые образуются при высоких окислительных условиях или в результате взаимодействия сильных окислителей. Они имеют большую степень окисления и обладают своими уникальными свойствами. Надеюсь, теперь вы лучше понимаете, что такое высшие оксиды и какие элементы могут их образовывать. Если у вас возникли еще вопросы, не стесняйтесь задать их!
Места увеличения высших оксидов
Одной из областей, где происходит увеличение высших оксидов, является окружающая среда. В процессе горения топлива, автомобильных выбросов, промышленных процессов и других источников, в атмосферу попадают различные газы и частицы, включая высшие оксиды. Повышенные концентрации высших оксидов, таких как диоксид азота и диоксид серы, оказывают негативное воздействие на окружающую среду и здоровье людей.
Еще одним местом увеличения высших оксидов является промышленность. Многие промышленные процессы, такие как производство стали, химическая обработка и производство электроэнергии, включают использование различных химических соединений, которые могут приводить к образованию высших оксидов в виде отходов или побочных продуктов. Повышенные концентрации высших оксидов в промышленных районах могут привести к загрязнению окружающей среды и негативно повлиять на здоровье работников и населения в этом районе.
Также, рассмотрим сельское хозяйство, где применяются различные виды удобрений для повышения урожайности растений. Некоторые из этих удобрений содержат высшие оксиды соединений азота. При неправильном использовании удобрений или избыточном накоплении высших оксидов в почве может возникать проблема загрязнения подземных вод и окружающей среды.
Наконец, высшие оксиды могут образовываться и в природной среде. Например, вулканическая активность, лесные пожары и другие природные процессы могут привести к повышенной концентрации высших оксидов в атмосфере и окружающей среде.
Раздел 3
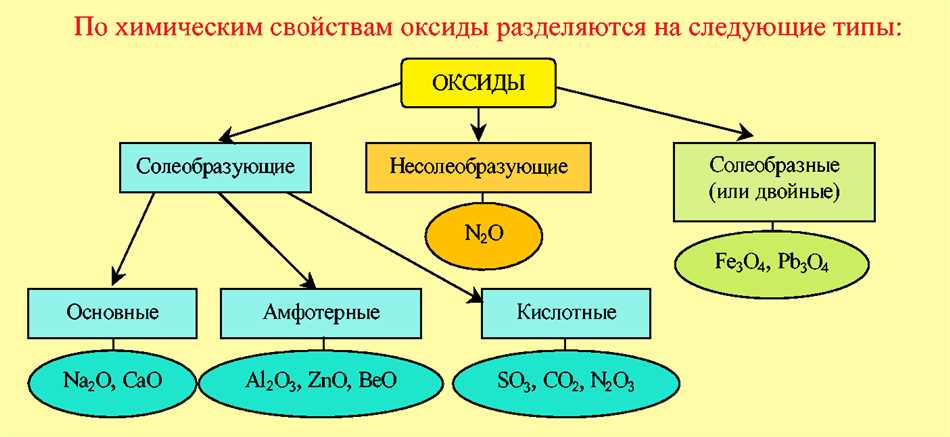
Теперь перейдем к рассмотрению представителей высших оксидов и местам, где они обнаруживаются наиболее часто. Ведь познание именно этих деталей поможет нам лучше понять, как высшие оксиды влияют на нашу жизнь и окружающую среду.
Один из главных представителей высших оксидов — диоксид углерода, или СО2. Его является безцветным и беззапахным газом, который образуется при сгорании топлива, а также является результатом дыхания и разложения органических веществ. Высокая концентрация СО2 обнаруживается в атмосфере, особенно в районах с большим промышленным загрязнением, на складах отходов и на автомагистралях.
Высшие оксиды еще находятся в составе загрязненной воды. Например, одним из представителей является азотная кислота – одна из самых сильных кислот. Она образуется в результате окисления азота в атмосфере и попадает в водные источники промышленным выбросом и сточными водами. Высокая концентрация азотной кислоты может вызвать серьезные проблемы для растений, животных и людей, поэтому очень важно контролировать выбросы данного вещества.
Представители высших оксидов:
- Диоксид углерода (СО2)
- Азотная кислота (HNO3)
- Сернистый ангидрид (SO2)
- Оксид азота (NO)
СО2, азотная кислота, сернистый ангидрид и оксид азота — все эти вещества встречаются в различных точках нашей планеты. Это может быть густые города с большим количеством промышленных предприятий, рядом с которыми содержание этих оксидов ощутимо повышено. Однако, к сожалению, высшие оксиды обнаруживаются и в таких изолированных местах, как даже удаленные от цивилизации области: леса, горы или океаны. Зато они не висят густыми облаками над этими областями, как часто можно себе воображать.
Таким образом, познакомившись с представителями высших оксидов и местами, где они чаще всего встречаются, мы можем лучше понять их значимость и влияние на нашу жизнь. Важно помнить, что контроль за выбросами высших оксидов и поддержание экологической сбалансированности — задача каждого из нас. Что Вы думаете по этому поводу?
Представители высших оксидов
Высшие оксиды характеризуются тем, что у элемента, кислорода, наиболее высокая степень окисления. Они обладают высокой электроотрицательностью и реактивностью, что делает их важными веществами для различных процессов и реакций.
Среди представителей высших оксидов можно выделить несколько важных элементов:
- Сера: сернистый ангидрид (SO2), сернистый триоксид (SO3), серный гексаоксид (SO6).
- Азот: диоксид азота (NO2), триоксид азота (NO3), тетраоксид азота (N2O4).
- Фосфор: пятиокись фосфора (P2O5), шеститриоксид фосфора (P2O6).
- Хлор: диоксид хлора (ClO2), триоксид хлора (ClO3), пятиокись хлора (Cl2O5).
Эти вещества имеют широкое применение в различных отраслях промышленности, таких как производство удобрений, пищевая промышленность, синтез органических соединений и другие.






