- Процесс щелочной реакции NaOH + H3PO4
- Натриевый гидроксид: состав и особенности
- Фосфорная кислота: основные свойства и применение
- Принципы щелочной реакции и ее проявление
- Результаты реакции NaOH + H3PO4
- NaOH + H3PO4 → Na3PO4 + H2O
- Факторы, влияющие на результат реакции
- Концентрация реагентов
- Взаимное соотношение реагентов
- Температура реакции
- Режим смешивания
- Практическое применение щелочной реакции NaOH + H3PO4
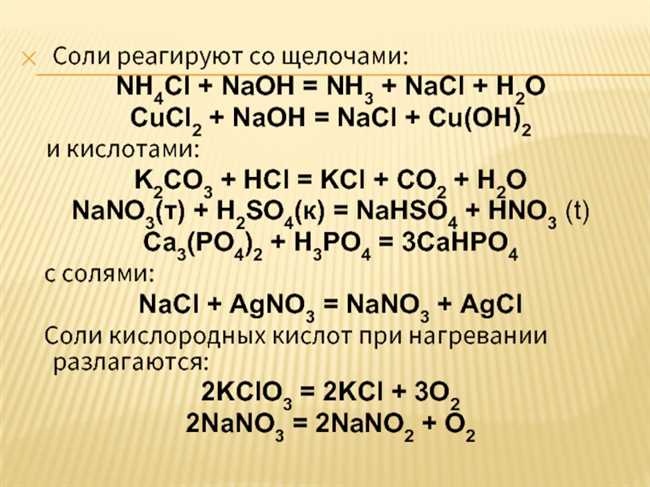
Щелочная реакция между гидроксидом натрия (NaOH) и фосфорной кислотой (H3PO4) является достаточно интересным процессом с различными результатами. Изначально, при смешивании NaOH и H3PO4 образуется моносолевой фосфата натрия (NaH2PO4), который является первым продуктом реакции. Тем не менее, данная реакция может также протекать дальше и образовывать дисолевой и трисолевой фосфаты натрия. Наибольшее количество ограничено концентрацией фосфорной кислоты и гидроксида натрия в начальной смеси. Это означает, что одну и ту же реакцию можно проталкивать в различные стороны, основываясь на начальных условиях. Эта щелочная реакция имеет множество промышленных и лабораторных применений и продолжает быть исследуемой для дальнейшего понимания ее особенностей и результатов.
Процесс щелочной реакции NaOH + H3PO4

На первый взгляд может показаться, что смешивание двух растворов – щелочного и кислотного – должно привести просто к нейтрализации, т.е. к образованию соли и воды. Однако, в данном случае реакция проходит несколько иначе.
Когда NaOH реагирует с H3PO4, происходит образование натрийфосфата (Na3PO4) и воды (H2O). Особенностью этой реакции является наличие нескольких гидроксильных групп в фосфорной кислоте, каждая из которых может реагировать с гидроксидом натрия.
Подчеркнуто стоит отметить, что щелочная реакция является экзотермической, т.е. сопровождается выделением тепла. Поэтому при смешивании NaOH и H3PO4 можно ощутить повышенную температуру и наблюдать выделение пара, что является характерным признаком процесса.
Важно помнить, что NaOH и H3PO4 являются крайне щелочным и кислым соединением соответственно. При проведении эксперимента нужно быть осторожным и соблюдать меры безопасности, так как оба вещества могут вызвать ожоги и повреждение тканей.
В итоге, реакция NaOH + H3PO4 приводит к образованию натрийфосфата и воды, проходит с выделением тепла и требует внимательности при выполнении. Такие щелочные реакции имеют важное значение в химической промышленности, в лабораторном анализе и в других приложениях.
Натриевый гидроксид: состав и особенности
Натриевый гидроксид (NaOH) состоит из трех элементов: натрия (Na), кислорода (O) и водорода (H). Вода, с добавлением которой происходит реакция соединения, является основным компонентом этих трех элементов. Интересно, что такое соединение имеет очень высокую растворимость в воде, что делает его очень удобным для использования в разных процессах.
Натриевый гидроксид широко применяется в промышленности, медицине и быту. Он используется для производства мыла, бумаги, пластиков, стекла и многих других продуктов. Это замечательное вещество также находит применение в качестве очистителя и обезжиривателя, благодаря своей щелочной природе.
Натриевый гидроксид является очень сильной основой и может быть опасным в обращении, поэтому необходимо соблюдать осторожность и работать с ним только в защитных средствах, таких как перчатки и очки. Кроме того, при работе с ним нужно соблюдать правила безопасности и производить вентиляцию помещения.
Теперь, когда ты знаешь о натриевом гидроксиде немного больше, расскажи мне, как ты думаешь, какие еще применения может иметь это вещество? Имеешь ли ты опыт работы с ним? Буду рад услышать твое мнение. До скорой встречи!
Фосфорная кислота: основные свойства и применение
Фосфорная кислота, или H3PO4, — это бесцветная жидкость, которая обладает высокой степенью кислотности. Она является трехосновной кислотой, что означает, что в ее молекуле содержится три замещенных атомами водорода атома кислорода. Интересно, не так ли?
Основными свойствами фосфорной кислоты являются ее кислотность и растворимость в воде. Она обладает оксидирующими свойствами и может реагировать с различными веществами, в том числе с металлами и основаниями.
Теперь давай поговорим о применении фосфорной кислоты. Она широко используется в различных отраслях, включая химическую промышленность, сельское хозяйство, пищевую промышленность и производство удобрений.
В химической промышленности фосфорная кислота используется для производства фосфорных соединений, таких как соли фосфорной кислоты, фосфорные эфиры и фосфаты. Они находят применение в производстве пластиков, детергентов, смазочных материалов и многое другое. Фосфорные соединения также используются в производстве горючих материалов и пиротехники.
Кроме того, фосфорная кислота играет важную роль в сельском хозяйстве. Она используется в качестве компонента удобрений, так как фосфор является одним из трех основных макроэлементов, необходимых для роста растений. Фосфатные удобрения вносятся в почву для повышения урожайности и качества растений.
Не забывай, что фосфорная кислота также используется в пищевой промышленности в качестве добавки для регулирования кислотности и антиокислительного средства. Она может применяться в производстве напитков, консервов, сыров и других пищевых продуктов.
Вот и все! Ты узнал(а) основные свойства фосфорной кислоты и ее применение. Надеюсь, ты насладился(ась) чтением и изучил(а) что-то новое. Не стесняйся задать вопросы, если у тебя есть!
Принципы щелочной реакции и ее проявление

Щелочная реакция — это химическая реакция, в которой щелочное соединение, такое как гидроксид натрия (NaOH), реагирует с кислотой, например, фосфорной кислотой (H3PO4), образуя соль и воду. В результате такой реакции образуется основание, которое обладает щелочной средой и характеризуется высоким pH-значением.
Процесс щелочной реакции основан на взаимодействии ионов гидроксида NaOH и ионов водорода H3PO4. Когда эти два соединения смешиваются, ионы гидроксида натрия и ионы водорода фосфорной кислоты реагируют друг с другом, образуя воду (H2O). В результате такой реакции образуется натрийфосфат (Na3PO4), который является солью.
Если вы когда-нибудь пользовались щелочным раствором, то наверняка заметили его специфические свойства. Щелочные растворы обладают высокой концентрацией гидроксидных ионов, что делает ихщелочной средой. Это приводит к ряду проявлений.
- Щелочные растворы имеют гладкую текстуру и обладают желтоватым или зеленоватым оттенком.
- Они также способны обезжиривать поверхности и разлагать жиры, поэтому часто используются в моющих средствах.
- Щелочные растворы обладают щелочным вкусом и способны вызывать покалывание на коже и слизистых оболочках.
- Они также изменяют цвет некоторых индикаторов, например, красного фенильного фталеина, который при контакте с щелочью становится фиолетовым.
Теперь вы, вероятно, зададите вопрос: «Зачем мне все это знать?». Ответ прост — знание основных принципов щелочной реакции позволит вам лучше понять окружающую нас химию и ее воздействие на нашу жизнь. Благодаря этим знаниям вы сможете сделать более обоснованный выбор, касающийся использования химических веществ в повседневной жизни.
Итак, не стоит бояться химии и химических реакций. Они являются важной частью нашей жизни и незаменимым инструментом для достижения многих целей. Поэтому продолжайте изучать химию и исследовать мир вокруг вас!
Результаты реакции NaOH + H3PO4
NaOH + H3PO4 → Na3PO4 + H2O
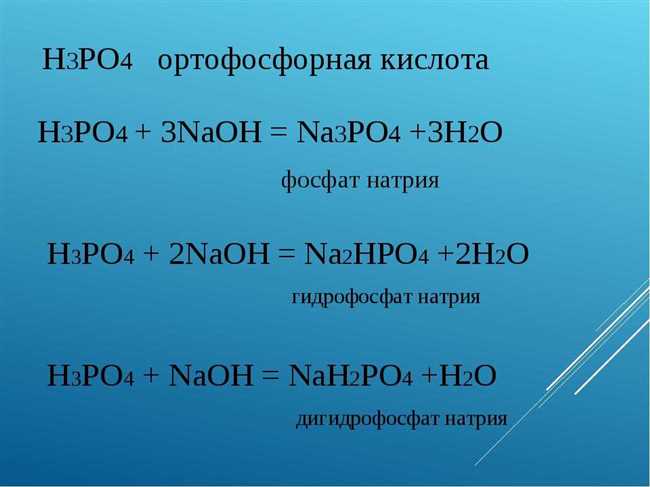
В результате этой реакции образуется раствор натрийфосфата и вода. Натрийфосфат является солью, которая обычно находится в виде белого кристаллического порошка.
Когда раствор NaOH встречает раствор H3PO4, постепенно начинает происходить реакция. Она может быть мгновенной или занимать некоторое время в зависимости от концентрации и температуры растворов. Обычно эта реакция происходит при комнатной температуре и занимает не более нескольких минут.
Натрийфосфат, образующийся в результате этой реакции, имеет различные применения. Он может использоваться в пищевой промышленности как добавка E339, в качестве удобрений для растений, а также в лабораторных и химических процессах.
Итак, результаты реакции между NaOH и H3PO4 включают образование натрийфосфата (Na3PO4) и воды (H2O). Эта реакция является типичным примером кислотно-щелочной нейтрализации и может использоваться в различных областях, включая пищевую промышленность и научные исследования.
Факторы, влияющие на результат реакции
Результаты реакции между щелочью (NaOH) и фосфорной кислотой (H3PO4) могут быть разнообразными и зависят от нескольких факторов. В данном случае, исходные реагенты это вода, гидроксид натрия (щелочь) и фосфорная кислота. Когда эти вещества смешиваются, происходит химическая реакция, результат которой можно предсказать, учитывая следующие факторы:
Концентрация реагентов
Концентрация реагентов играет важную роль в реакции между NaOH и H3PO4. Если концентрация реагентов высокая, то вероятность их взаимодействия и реакции будет больше. Таким образом, при высокой концентрации NaOH и H3PO4 можно ожидать, что реакция будет проходить активнее и с большим образованием продуктов.
Взаимное соотношение реагентов
Отношение между NaOH и H3PO4 также влияет на результаты реакции. Если соотношение между реагентами соответствует стехиометрии, то можно ожидать полного расхода реагентов и образования соответствующих продуктов. Однако, если одного из реагентов (NaOH или H3PO4) будет слишком много или слишком мало, то реакция может протекать не полностью и образовываться будут лишь частично продукты.
Температура реакции
Температура также играет свою роль в реакции между NaOH и H3PO4. Повышение температуры обычно ускоряет химические реакции, включая данную. Это связано с тем, что при повышении температуры увеличивается коллизия между молекулами реагентов, что способствует их взаимодействию и образованию продуктов.
Режим смешивания
Режим смешивания, или скорость смешивания реагентов тоже может повлиять на результат реакции. Если реагенты быстро смешиваются, то зона их взаимодействия будет больше, что повышает вероятность реакции и образования продуктов.
Таким образом, концентрация реагентов, взаимное соотношение реагентов, температура реакции и режим смешивания – это основные факторы, которые влияют на результаты реакции между щелочью и фосфорной кислотой. Рассмотрение и учет этих факторов позволяет более точно предсказать и контролировать химическую реакцию.
Практическое применение щелочной реакции NaOH + H3PO4
Щелочная реакция между гидроксидом натрия (NaOH) и фосфорной кислотой (H3PO4) имеет широкий спектр применений в различных отраслях науки и техники. Результаты и особенности этой реакции играют важную роль в разработке новых материалов, производстве химических продуктов и поддержании определенных условий в ряде процессов.
Основные применения щелочной реакции NaOH + H3PO4 включают:
- Производство удобрений: Фосфатные удобрения являются одним из основных продуктов, получаемых в результате реакции между гидроксидом натрия и фосфорной кислотой. Эти удобрения содержат необходимые растениям минералы, такие как фосфор, что способствует повышению урожайности и качества сельскохозяйственных культур.
- Производство чистящих средств: Щелочная реакция NaOH + H3PO4 также используется для производства различных химических продуктов, включая чистящие средства. Гидроксид натрия и фосфорная кислота взаимодействуют, образуя соли, которые могут быть использованы для удаления загрязнений и накипи на различных поверхностях.
- Производство бумаги: Фосфатные соединения, полученные в результате реакции между NaOH и H3PO4, могут быть использованы в производстве бумаги. Эти соединения способствуют улучшению качества бумаги и повышению ее прочности.
- Регулирование pH: Щелочная реакция NaOH + H3PO4 может быть использована для регулирования pH в различных процессах. Полученный продукт – фосфатная соль – может служить стабилизатором и помогать поддерживать определенное значение pH.
Описанная щелочная реакция имеет большое значение в различных областях промышленности и научных исследований. Использование ее результатов и особенностей позволяет разрабатывать новые материалы, улучшать процессы производства и поддерживать необходимые условия в различных отраслях.






