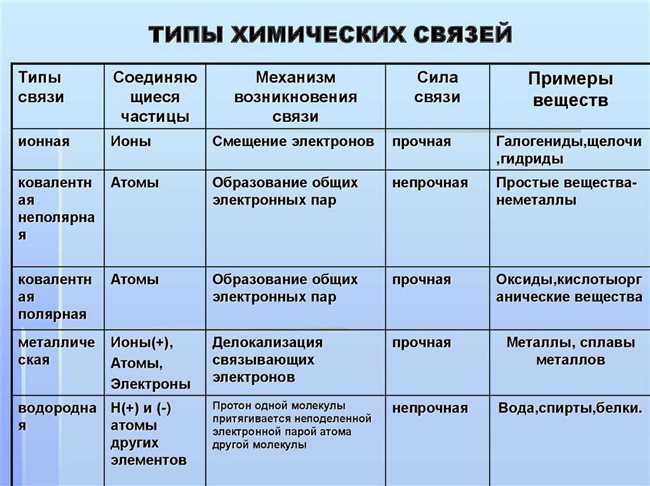
В химии существуют различные вещества, которые содержат двойные связи между атомами. Одним из примеров таких веществ являются алкены, которые содержат двойную связь между углеродными атомами. Эта двойная связь образуется, когда два атома углерода делят между собой четыре электрона, в результате чего образуется плоское кольцевое образование.»Жирные кислоты также содержат двойные связи между углеродными атомами. Молекулы жиров состоят из глицерина (трехвалентного спирта) и трех молекул жирных кислот, каждая из которых содержит две или более двойных связей.»
Двойная связь в химии играет важную роль и может влиять на свойства вещества. Она обусловливает реакционную активность, структуру и физические свойства вещества. Понимание механизма образования и поведения двойной связи помогает ученым исследовать химические реакции, разрабатывать новые материалы и прогнозировать свойства веществ.
Примеры веществ
Другим примером вещества является кислород. Кислород является одним из элементов периодической таблицы и имеет символ O. Он составляет около 21% атмосферы Земли и необходим для существования живых организмов. Кислород также используется в процессе горения и дыхания.
Примеры веществ с двойными связями
Одним из ключевых понятий в химии является двойная связь. Это связь между двумя атомами, в которой используются две пары электронов. Двойная связь может образоваться между атомами различных элементов и обладает особыми свойствами.
Примером вещества с двойной связью является этилен. Этилен — это газообразное соединение, состоящее из двух атомов углерода и четырех атомов водорода. Он широко используется в промышленности в качестве сырья для производства пластмасс, резиновых изделий и синтетических волокон.
Еще одним примером вещества с двойной связью является этиловый спирт, или этанол. Этанол — это спирт, который используется в различных отраслях, включая медицину, промышленность и бытовые цели. Двойная связь в молекуле этанола делает его реактивным и способным участвовать в различных химических реакциях.
Также можно привести примеры веществ с двойными связями, таких как ацетилен, бензол и стеариновая кислота. Все эти вещества используются в различных областях и имеют свои особенности и свойства, связанные с наличием двойных связей.
Заключение
Примеры веществ, которые мы рассмотрели, являются всего лишь небольшой частью многообразия химических соединений. Важно помнить, что каждое вещество имеет свои уникальные свойства и возможности, и именно эти свойства делают их ценными и полезными в различных сферах нашей жизни.
Вещества со свободной двойной связью
В химии существуют различные вещества, которые обладают свободной двойной связью. Это особое свойство, которое делает эти вещества особенными и интересными.
Для начала разберемся, что такое двойная связь. В молекулах химических веществ атомы связываются друг с другом для образования структуры вещества. Однако, в некоторых случаях атомы могут образовывать не одну, а две связи. Это и называется двойной связью. Атомы, образующие двойную связь, обычно делят между собой два электрона.
Одним из примеров веществ со свободной двойной связью является этилен. Это газообразное вещество, часто используемое в промышленности для производства пластмасс. У этилена две свободные двойные связи между атомами углерода. Это делает его очень реакционноспособным и позволяет использовать его для создания различных соединений.
Еще одним примером вещества со свободной двойной связью является ацетилен. Это газообразное вещество, сильно горючее и используемое в сварке и резке металла. Ацетилен также обладает двумя свободными двойными связями между атомами углерода, что делает его очень реакционноспособным.
Свободная двойная связь позволяет молекулам создавать сложные структуры и участвовать в различных химических реакциях. Например, этилен может образовывать полимеры, такие как полиэтилен, который широко используется в производстве пластмассовых изделий.
Интересно, что свободная двойная связь может быть не только у углерода, но и у других элементов, таких как азот и кислород. Такие элементы также могут образовывать различные вещества с уникальными свойствами.
Вещества с ароматическими циклами
Одним из наиболее известных примеров веществ с ароматическими циклами является бензол (C6H6). Бензол имеет шесть атомов углерода, расположенных в форме шестиугольного кольца. Из-за уникальной структуры, бензол обладает характерным сладким запахом и используется в производстве пластмасс, резиновых изделий и веществ, используемых в фармацевтической промышленности.
Другие примеры веществ с ароматическими циклами включают толуол, нафталин и антрацен. Толуол (C7H8) является производным бензола и используется в производстве лаков, красителей и растворителей. Нафталин (C10H8) также известен своим характерным запахом и используется в составе маскирующих и ароматических веществ, а также в производстве моющих средств. Антрацен (C14H10) используется в производстве красителей и как смазочное вещество.
Понимание механизма образования ароматических циклов и их свойств является важным для развития новых материалов и лекарственных препаратов. Многие вещества с ароматическими циклами проявляют непредсказуемые поведение и синтез новых средств с такими структурами требует глубокого понимании химических реакций и свойств этих веществ.
Примеры веществ с ароматическими циклами:

- Бензол
- Толуол
- Нафталин
- Антрацен
Химия ароматических циклов продолжает развиваться, и новые соединения с такими структурами постоянно открываются. Эти соединения имеют огромный потенциал в области новых материалов, лекарств и энергетических исследований.
Такие вещества, как бензол, толуол, нафталин и антрацен, являются лишь некоторыми примерами веществ с ароматическими циклами. Структуры и свойства этих соединений делают их особенно интересными для научных исследований и промышленности. Ароматические соединения являются одной из фундаментальных основ химии и продолжают вдохновлять нас своими удивительными свойствами и возможностями.
Вещества с конъюгированными двойными связями
В химии существует класс веществ с особенной структурой, называемой конъюгированными двойными связями. Эти вещества имеют несколько смежных двойных связей, расположенных вместе в одной молекуле. Они представляют собой уникальные химические соединения с интересными свойствами.
Одним из основных свойств конъюгированных двойных связей является их способность образовывать систему конъюгации. Конъюгация — это электронное взаимодействие между соседними пи-орбиталями двойных связей, которое делает эти соединения стабильными и позволяет им проявлять разнообразные химические и физические свойства.
Одним из примеров веществ с конъюгированными двойными связями являются конъюгированные диены. Это органические соединения, содержащие две смежные двойные связи в углеводородной цепи. Примером такого вещества может служить бутадиен (1,3-бутадиен), молекула которого содержит две смежные двойные связи и является одной из самых простых и наиболее изученных соединений.
Конъюгированные диены обладают несколькими интересными свойствами. Например, они могут подвергаться реакции электроциклического протекания, когда электронная плотность в системе конъюгации перемещается по молекуле. Это явление может приводить к образованию новых соединений с разными свойствами. Кроме того, молекулы конъюгированных диенов могут обладать уникальными оптическими свойствами, что делает их полезными для применения в области оптических материалов и устройств.
Другим примером веществ с конъюгированными двойными связями являются азодиарены. Это класс органических соединений, содержащих центральный азотный атом и два ароматических кольца, связанных с ним конъюгированными двойными связями. Азодиарены обладают яркими красящими свойствами, благодаря которым они широко используются в промышленности для окрашивания различных материалов.
Вещества с кумулятивными двойными связями
Кумулятивная двойная связь возникает между атомами, когда два атома соседних углеродных атомов разделяют общий путь. В результате образуется структура, в которой атомы соединены не только двойной связью, но также множеством пи-связей. Такая связь может быть представлена в виде цепочки атомов с кратными связями между ними, образуя особую структуру.
Примерами веществ с кумулятивными двойными связями являются аллены, цумарены и иксимены. Аллены обладают структурой, в которой два углеродных атома связаны двумя двойными связями и дополнительными одинарными связями со смежными атомами. Цумарены представляют собой ароматические соединения, в которых два углеродных атома связаны двумя двойными связями и имеют по три пи-электрона в области пи-электронных облаков. Иксимены состоят из трехкратно связанных атомов кремния и кислорода.
Образование кумулятивных двойных связей является результатом особых электронных структур и лежит в основе различных физических и химических свойств этих веществ. Химики активно изучают кумулятивные двойные связи и их влияние на реакционную способность и реакционные механизмы данных веществ.






