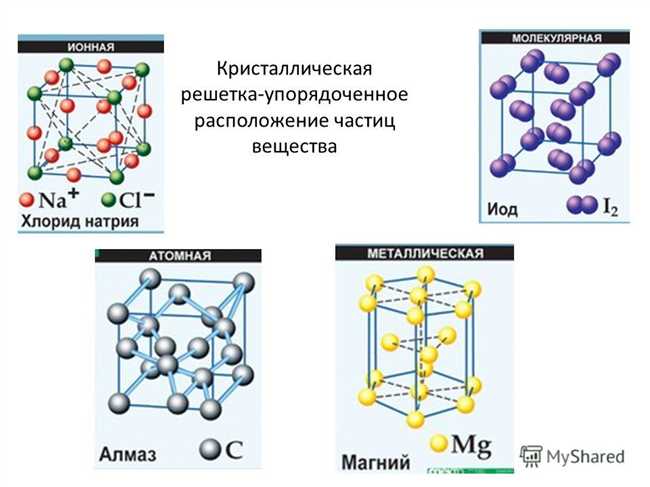
P2O5 – это химическое соединение, состоящее из двух атомов фосфора и пяти атомов кислорода. Оно является оксидом фосфора(V) и представляет собой один из важных ингредиентов в производстве удобрений, стекла и керамики. Связи в P2O5 являются ионными и ковалентными, что делает это соединение необычайно реакционным. Кристаллическая решетка P2O5 имеет моноклинную симметрию и состоит из полимерных цепочек, в которых атомы фосфора и кислорода чередуются. Это обеспечивает устойчивость и прочность решетки, делая P2O5 важным компонентом во многих промышленных процессах.
Тип связи в P2O5

Один из ключевых аспектов при рассмотрении типа связи в P2O5 — это то, что химическую формулу можно трактовать как соединение между непарными валентными электронами атомов фосфора и кислорода. Валентные электроны — это электроны, участвующие в образовании химической связи между атомами.
Теперь давайте обратимся к основным типам связей, которые могут быть представлены в P2O5:
- Ионная связь: предполагает передачу электронов от одного атома к другому, образуя ионы положительного и отрицательного заряда. Однако в случае P2O5, ионная связь маловероятна, поскольку оба элемента, фосфор и кислород, обладают валентностью, что означает, что они имеют возможность образовывать ковалентные связи, где электроны не переносятся полностью, а распределяются между атомами.
- Ковалентная связь: ковалентная связь возникает при совместном использовании (перекрестном передаче) электронов между двумя атомами. P2O5 обладает ковалентной связью между атомами фосфора и кислорода, где электроны делятся между ними.
Итак, исходя из анализа выше, можно заключить, что связь в P2O5 представлена главным образом ковалентной связью. Эта информация важна для понимания свойств и реакций P2O5.
Я надеюсь, что данная информация помогла вам лучше понять тип связи в P2O5. Не стесняйтесь задавать вопросы, если что-то осталось неясным!
Ковалентная связь
Когда атомы образуют ковалентную связь, они становятся взаимозависимыми и образуют молекулу. Важно отметить, что ковалентные связи могут образовываться только между неметаллическими элементами, так как они имеют тенденцию привлекать электроны и образовывать общую область электронной оболочки.
Одной из особенностей ковалентной связи является ее прочность. Атомы, образующие ковалентную связь, делят свои электроны таким образом, чтобы достичь наиболее стабильного состояния с полностью заполненными или полностью пустыми внешними энергетическими уровнями. Это позволяет ковалентным связям быть очень сильными и стабильными.
Стоит отметить, что в ковалентной связи электроны могут быть разделены неравномерно, создавая полярную ковалентную связь. В такой связи один атом притягивает электроны больше, чем другой, создавая разность электрического заряда и поляризуя молекулу. Это дает возможность образованию диполя и таким образом создает электрическое взаимодействие между молекулами.
Ковалентная связь является одной из основных причин существования различных веществ и материалов в нашем мире. Она отвечает за образование молекул, которые, в свою очередь, образуют все от живых организмов до неорганических веществ. Например, ковалентная связь между атомами водорода и атомом кислорода образует молекулу воды, которая является основным компонентом жизни.
Так что следующий раз, когда вы употребляете слово «вода» или наблюдаете за дождем, помните, что все это возможно благодаря ковалентной связи. Она связывает атомы и создает всю красоту и разнообразие мира, в котором мы живем.
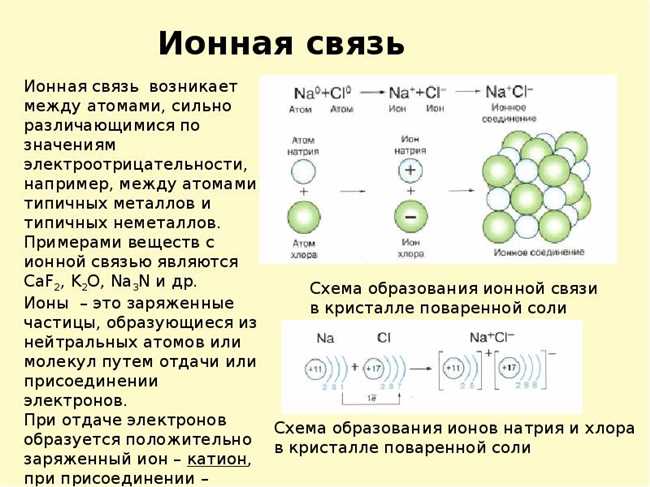
Ионная связь
Ионная связь — это тип химической связи, которая образуется между положительно и отрицательно заряженными ионами. Она является результатом притяжения этих частиц друг к другу.
Когда атомы или молекулы приходят в контакт друг с другом, они либо отталкиваются, либо притягиваются друг к другу. В случае ионной связи, происходит именно притяжение ионов с противоположными зарядами. Как это происходит?
- Один атом отдает один или несколько электронов, становясь положительно заряженным ионом (катионом).
- Другой атом получает эти электроны, становясь отрицательно заряженным ионом (анионом).
- Затем возникает притяжение между положительно и отрицательно заряженными ионами, образуя устойчивый кристаллический решетку.
Ионная связь обычно возникает между металлическими элементами (которые отдают электроны) и неметаллическими элементами (которые получают электроны).
Ионная связь имеет несколько ключевых характеристик:
- Сильная: ионная связь обладает высокой прочностью, что делает ее стойкой к температурным и давлению воздействиям.
- Кристаллическая решетка: ионы в ней располагаются в определенном порядке, образуя трехмерную структуру.
- Неполярность: ионная связь создает неполярные соединения, так как электронная плотность между ионами равномерно распределена.
- Легко разрушаемая: ионная связь легко разрушается в растворах или при нагревании, поэтому соединения с ионной связью растворяются в воде или плавятся при низких температурах.
Ионная связь имеет огромное значение для нашей повседневной жизни. Например, она играет ключевую роль в формировании солей, таких как столовая соль, которые мы используем в пище и для консервации продуктов. Также, ионная связь обеспечивает структуру и прочность веществ, таких как кристаллические минералы и камни.
Итак, ионная связь — это мощная и устойчивая химическая связь, которая образуется между положительно и отрицательно заряженными ионами через притяжение. Она обладает высокой прочностью и создает кристаллическую решетку. Используется в различных областях, включая пищевую промышленность и геологию, и является неотъемлемым элементом нашей повседневной жизни.
Металлическая связь
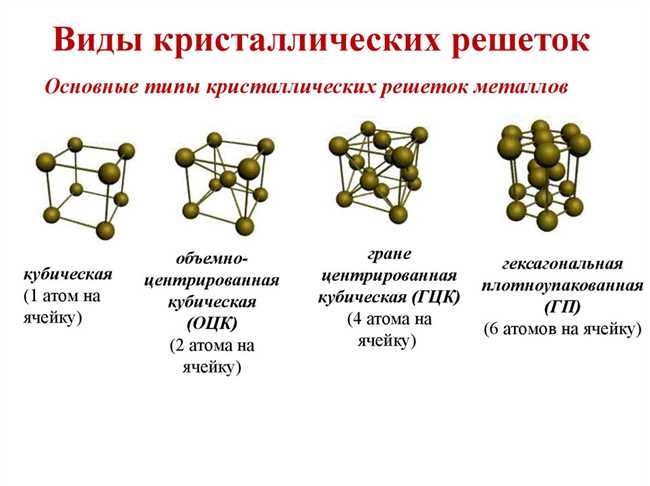
Металлические связи возникают между атомами металла, и они играют решающую роль в структуре искусственных и природных металлов. Эти связи обладают невероятной прочностью и эластичностью, что делает металлы такими прекрасными материалами для различных конструкций и механизмов. Именно благодаря металлической связи мы можем строить надежные здания, производить прочные автомобили и создавать многое другое.
Одной из ключевых особенностей металлической связи является ее подвижность. В металлических кристаллах атомы могут свободно перемещаться и менять свои позиции, что придает металлу способность проводить электричество и тепло. Как ты уже мог догадаться, именно благодаря этому свойству металлы широко используются в сфере электричества и электротехники.
Целая система взаимодействий
Понимание металлической связи – это сложная и увлекательная наука. Объединение атомов в металлической связи является результатом взаимодействия между положительно заряженными ядрами и свободными электронами. Эти электроны, называемые «электронами свободного движения», не привязаны к конкретным атомам и способны свободно перемещаться по всей металлической структуре.
Интересно, не правда ли? Но на этом интерес не заканчивается. Кроме свободных электронов, в металлической связи также участвуют электроны, занятые внутренними оболочками атомов. Их взаимодействие с положительно заряженными ядрами и свободными электронами приводит к устойчивости металлической решетки и ее свойствам.
Уникальные свойства металлов
Как я уже отметил ранее, металлическая связь обеспечивает металлам множество уникальных свойств. Во-первых, она обеспечивает высокую теплопроводность и электропроводность металлов. Во-вторых, металлическая связь придает металлам способность легко подвергаться пластической деформации, что делает их идеальными для процессов ковки и проката. А еще металлы благодаря связи могут быть импервиусными к газам и жидкостям.
Спасибо, что прочитал этот текст! Надеюсь, он был полезен и интересен для тебя. Металлическая связь – это действительно удивительное явление, которое играет огромную роль в нашей жизни. Как ты считаешь, какие сферы деятельности были бы невозможны без металлической связи? Поделись своими мыслями в комментариях!
Кристаллическая решетка P2O5
P2O5 — это химическая формула фосфорного пентоксида, который образует ковалентную связь между атомами фосфора и кислорода. Кристаллическая решетка P2O5 имеет аморфную структуру, то есть ее атомы не расположены в строго упорядоченном порядке.
Тип связи:
P2O5 обладает ковалентной связью, которая формируется между атомами фосфора и кислорода. Ковалентная связь характеризуется общим использованием электронных пар двумя атомами, что придает структуре P2O5 высокую степень устойчивости.
Кристаллическая решетка:
Кристаллическая решетка P2O5 не обладает простой упорядоченной структурой, как у большинства кристаллических веществ. Она представляет собой аморфную, случайную композицию атомов фосфора и кислорода, которые расположены в непредсказуемом порядке.
В целом, кристаллическая решетка P2O5 представляет собой сложный объект изучения, который требует дальнейших исследований для полного понимания его свойств и потенциальных применений в различных отраслях науки и техники.






