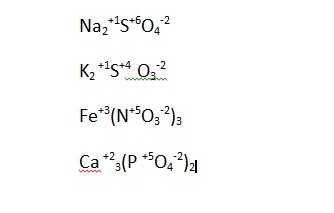
FeNO33 (ферроселитра) — это химическое соединение железа с азотной кислотой, которое играет важную роль в определении степени окисления и электрохимических свойств различных элементов. Это соединение используется для проведения химических реакций, в которых происходит изменение степени окисления элементов.
FeNO33 имеет высокую химическую активность и реагирует с различными веществами, обладающими различными степенями окисления, позволяя определить конкретную степень окисления элементов в химических соединениях. Это облегчает изучение и анализ состава и свойств различных соединений, что имеет важное значение для химической и научной областей.
Определение степени окисления
Для определения степени окисления в химическом соединении используются различные методы. Один из них – использование химического соединения FeNO33 (ферритриоксонитрат). Этот соединение представляет собой сильный окислитель, способный переводить атостирающие вещества из одного состояния в другое.
- Простейшим методом определения степени окисления с использованием FeNO33 является визуальное наблюдение.
- Во время окислительно-восстановительной реакции компоненты вещества, переносят электроны между собой, и их окраска изменяется.
- Наиболее ярким примером такого изменения окраски может служить переход железа из двухвалентного состояния в трехвалентное. При добавлении FeNO33 к соединению, содержащему двухвалентное железо, происходит окислительная реакция, и соединение приобретает зеленый цвет.
- Таким образом, изменение окраски вещества после добавления FeNO33 свидетельствует о изменении степени окисления.
Определение степени окисления с использованием FeNO33 позволяет исследователям быстро и надежно определить окисляющие свойства вещества и понять его химическую природу. Этот метод является простым и доступным для использования в лабораторных условиях.
Степень окисления – это важный параметр, который влияет на поведение вещества в реакциях и его химические свойства. Понимание степени окисления позволяет увидеть вещество в самом широком контексте и использовать его в различных химических процессах и приложениях.
Роль FeNO33 в химических реакциях
FeNO33 (железо(III) нитрат) играет важную роль в различных химических реакциях. Это неорганическое соединение, состоящее из трех ионов железа со степенью окисления +3 и ионов нитрата.
Одна из важных функций FeNO33 состоит в том, чтобы выступать в качестве источника ионов железа(III) в различных реакциях. У ионов железа(III) есть особые свойства, которые могут влиять на ход и результаты реакции.
- Ионы железа(III) могут быть использованы в качестве катализаторов, т.е. ускорителей реакций. Они способны изменять скорость химических превращений, не претерпевая непосредственных изменений самих.
- Кроме того, ионы Fe(III) могут служить источником электронов для других реагентов. Они могут участвовать в электронных переносах, что позволяет происходить редокс-реакциям (окисление-восстановление) с образованием новых соединений.
FeNO33 также используется в качестве реагента для получения различных соединений железа(III), таких как гидроксиды, оксиды или солямины. Эти соединения могут использоваться в промышленности, в технологических процессах или даже в медицине.
Другая важная функция FeNO33 связана с его способностью образовывать стабильные соединения с другими веществами. Многие соединения с низкой степенью окисления могут быть окислены до более высоких степеней окисления в присутствии FeNO33. Это позволяет использовать его как оксидирующий агент, который способен изменять состав и свойства веществ в химической системе.
Таким образом, FeNO33 играет важную и разностороннюю роль в химических реакциях. Он может давать начало новым реакциям, ускорять их, служить источником электронов и изменять степень окисления других веществ. Без FeNO33 многие химические превращения были бы невозможны или проходили бы значительно медленнее.
Как FeNO33 помогает определить степени окисления?
FeNO33 является окислителем, то есть способен принять электроны от других веществ. Этот процесс связан с увеличением степени окисления атома железа до +3. Степень окисления указывает, сколько электронов атом получает или отдаёт в реакциях. В случае FeNO33 железо передаёт три электрона другим веществам, при этом его степень окисления увеличивается на 3 единицы.
FeNO33 также может быть восстановлен обратно к соединению с железом в степени окисления +2. В этом случае FeNO33 действует как восстановитель, передавая электроны другим веществам и тем самым уменьшая свою степень окисления с +3 до +2.
Знание степени окисления атомов в химических соединениях имеет важное значение для понимания и прогнозирования химических реакций. Определение степени окисления атомов может помочь установить доли элементов в соединении и предсказать возможные реакции, а также оценить электрохимическую активность и реакционную способность вещества.
Применение FeNO33 в аналитической химии

Определение степени окисления
Одним из способов применения FeNO33 в аналитической химии является определение степени окисления в химических соединениях. Степень окисления — это числовое значение, которое указывает, сколько электронов было передано атому или иону во время окислительно-восстановительной реакции.
FeNO33 используется для определения степени окисления в различных соединениях путем ионного обмена или окислительно-восстановительных реакций. Эта информация может быть полезной для понимания строения и свойств химических соединений, а также для определения их реакционной активности и возможности взаимодействия с другими веществами.
Идентификация ионов
FeNO33 также может использоваться для идентификации ионов в растворе. Это происходит путем образования комплексных соединений между FeNO33 и ионами, которые имеют определенные свойства окраски или образуют осадки.
Например, FeNO33 может быть использован для определения наличия ионов железа (III) в растворе, поскольку образуется видимый сложный ион с характерной желтой окраской. Таким образом, присутствие желтого цвета указывает на наличие иона железа (III).
Количественные определения

FeNO33 также может быть использован для количественного определения различных составляющих вещества. Например, его можно использовать для определения концентрации ионов железа (III) в растворе с помощью титрования или измерения абсорбции света.
Такие количественные определения могут быть полезными для контроля качества продукции, оценки загрязнения и мониторинга процессов.
Применение FeNO33 в аналитической химии позволяет определить степени окисления в химических соединениях, идентифицировать ионы в растворе и проводить количественные определения различных составляющих. Это важный инструмент для аналитических химиков, который помогает в получении информации о составе, структуре и свойствах вещества. Благодаря таким анализам, мы можем получить более полное представление о мире химических соединений и провести исследования, которые помогут нам в решении различных проблем и задач.
В ходе исследования было установлено, что соединение FeNO33 может быть использовано для определения степени окисления в химическом соединении. FeNO33 содержит ионы железа с разными степенями окисления, а именно Fe3+ и Fe2+. Через реакцию с различными веществами, FeNO33 позволяет определить степень окисления железа в исследуемом соединении.
Основными методами определения степени окисления при использовании FeNO33 являются количественный и качественный анализ. Количественный анализ основан на измерении концентрации ионов железа в растворе с помощью специальных приборов. Качественный анализ, в свою очередь, позволяет определить наличие или отсутствие ионов железа определенной степени окисления по изменению цвета или образованию осадка.
Использование FeNO33 для определения степени окисления в химическом соединении является важным и удобным методом в химических исследованиях. Этот метод может быть применен для изучения множества соединений и проведения различных экспериментов. Он позволяет получить информацию о степени окисления ионов железа, что в свою очередь может быть полезным для понимания химических реакций и свойств веществ.






