- Определение степени окисления хрома и выяснение Cr2SO43: полезные действия и советы
- Что такое степень окисления?
- Определение степени окисления хрома
- Пример: Cr2SO43
- Полезные действия и советы
- Раздел 1. Основные понятия
- Хром
- Окисление и степень окисления
- Сульфат
- Cr2SO43
- Раздел 2. Методы определения степени окисления хрома
- Раздел 3. Химический состав Cr2(SO4)3
- Раздел 4. Практическое применение и советы
- 1. Используйте метод периодной системы
- 2. Учитывайте суммарный заряд соединения
- 3. Обратите внимание на окружающую среду

Как определить степень окисления хрома и выяснить Cr2(SO4)3: полезные действия и советы
Вы, вероятно, знаете, что хром может существовать в различных окислительных состояниях. Но как точно определить степень окисления хрома и выяснить формулу Cr2(SO4)3? В данной статье мы рассмотрим несколько полезных действий и советов, которые помогут вам справиться с этой задачей.
Во-первых, для определения степени окисления хрома, вы можете использовать правила степеней окисления. Например, степень окисления хрома в Cr2(SO4)3 можно определить, зная, что в соединении сульфата ион имеет заряд -2, и суммарный заряд молекулы соединения равен нулю.
Во-вторых, можно провести анализ химической формулы Cr2(SO4)3. В данном случае, Cr указывает на присутствие двух атомов хрома, а (SO4)3 говорит о трех группах сульфата. Комбинируя эту информацию, можно определить формулу Cr2(SO4)3.
Следуя этим полезным действиям и советам, вы сможете успешно определить степень окисления хрома и разобраться с составом Cr2(SO4)3.
Определение степени окисления хрома и выяснение Cr2SO43: полезные действия и советы
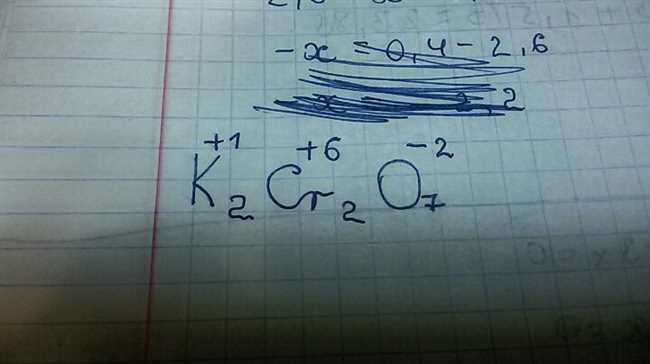
Что такое степень окисления?
Степень окисления (СО) — это числовое значение, которое отражает изменение числа электронов, переданных в процессе окислительно-восстановительной реакции. Рассмотрим пример с хромом, чтобы лучше понять, как определить его степень окисления.
Определение степени окисления хрома

Хром имеет различные степени окисления, например +2, +3 и +6. Для определения степени окисления хрома в хромсодержащем соединении воспользуемся следующими правилами:
- В простых соединениях хром имеет степень окисления +3. Например, CrCl3 или Cr2O3.
- В оксидах хрома, в которых как кислород, так и хром имеют отрицательные степени окисления, их сумма равна степени окисления хрома. Например, в Cr2O3 кислород имеет степень окисления -2, поэтому для Cr степень окисления будет +3.
- В кислородсодержащих соединениях степень окисления кислорода принимается равной -2. Например, в SO4 степень окисления кислорода равна -2.
- Сумма степеней окисления всех элементов в соединении равна нулю. Например, в хромсодержащем соединении с серой Cr2SO43, степень окисления хрома будет равна +6.
Пример: Cr2SO43
- Степень окисления кислорода в SO4 равна -2;
- Сумма степеней окисления серы и кислорода должна быть равна нулю: x + (-2) * 3 = 0;
Из этого можно вывести, что степень окисления хрома в Cr2SO43 равна +6. Таким образом, Cr2SO43 представляет собой хромсодержащее соединение с шестивалентным хромом.
Полезные действия и советы
Теперь, когда ты знаешь, как определить степень окисления хрома и применить это знание к примеру Cr2SO43, у тебя есть возможность лучше понять состав и свойства хромсодержащих соединений, а также использовать эти знания в химических исследованиях или практической деятельности.
Важно помнить, что определение степени окисления хрома основано на определенных правилах и правильная интерпретация этих правил поможет тебе получить точные результаты. Кроме того, при работе с хромсодержащими соединениями необходимо соблюдать меры безопасности и следовать указаниям по хранению и использованию вещества.
Уверен, что сейчас ты стал еще более осведомленным вопросе определения степени окисления хрома и примере Cr2SO43! Если у тебя возникли дополнительные вопросы, не стесняйся задавать их и продолжай развиваться в области химии и науки в целом. Удачи тебе в твоих исследованиях и экспериментах!
Раздел 1. Основные понятия
Хром
Окисление и степень окисления
Окисление — это процесс, при котором атом или ион теряет электроны, а степень окисления — это числовое значение, которое отражает, сколько электронов атом или ион в процессе окисления приобретает или теряет.
Сульфат
Сульфат — это соединение сульфатной кислоты с металлом или ионом. Сульфаты широко используются в различных отраслях, таких как производство удобрений, лекарств и косметики.
Cr2SO43
Cr2SO43 обозначает соединение хрома с сульфатной кислотой, в котором два атома хрома связаны с тремя атомами серы и четырьмя атомами кислорода. Чтобы определить степень окисления хрома в этом соединении, необходимо знать степени окисления серы и кислорода. В данном случае, сера имеет степень окисления -2, а кислород -2.
Чтобы определить степень окисления хрома, можно использовать следующее уравнение:
- 2х + 3(-2) + 4(-2) = 0
где х — степень окисления хрома.
Решая это уравнение, получаем:
- 2х — 6 — 8 = 0
- 2х — 14 = 0
- 2х = 14
- х = 7
Таким образом, степень окисления хрома в соединении Cr2SO43 равна +7.
Надеюсь, эта информация была полезной для вас! Если у вас есть еще вопросы, не стесняйтесь задавать!
Раздел 2. Методы определения степени окисления хрома
1. Метод перманганатной окислительной емкости
Одним из наиболее распространенных методов определения степени окисления хрома является метод перманганатной окислительной емкости. Суть метода заключается в том, что перманганат исходно имеет степень окисления +7, а хром -1. Путем титрования можно определить количество перманганата, необходимое для окисления хрома до более высокой степени окисления. Таким образом, можно определить степень окисления хрома.
2. Метод потенциометрического титрования
Другим эффективным методом определения степени окисления хрома является метод потенциометрического титрования. Этот метод основан на измерении изменения потенциала при добавлении окислителя (например, перманганата) в раствор соединения хрома. С помощью специальной аппаратуры и электродов можно точно определить момент, когда происходит окисление хрома и определить его степень окисления.
3. Метод спектрофотометрии
Спектрофотометрия — это метод определения концентрации вещества путем измерения поглощения или пропускания света. Для определения степени окисления хрома можно использовать метод спектрофотометрии. В данном случае изучается спектр поглощения соединения хрома в видимой области спектра. Измеряя поглощение на определенной длине волны, можно определить степень окисления хрома.
- Метод перманганатной окислительной емкости позволяет определить степень окисления хрома путем титрования перманганатом.
- Метод потенциометрического титрования основан на изменении потенциала при добавлении окислителя в раствор хрома.
- Метод спектрофотометрии используется для измерения поглощения света соединением хрома в видимой области спектра.
Выбор метода определения степени окисления хрома зависит от конкретной ситуации и доступных инструментов и реагентов. Важно правильно подобрать метод, чтобы получить точные и надежные результаты.
Раздел 3. Химический состав Cr2(SO4)3
Давайте поговорим о химическом составе соединения Cr2(SO4)3, чтобы лучше понять его свойства и действие.
Начнем с того, что Cr2(SO4)3 — это понятное обозначение соединения, в котором у нас есть хром (Cr) и сульфат (SO4) в составе.
Чтобы более точно определить степень окисления хрома в этом соединении, нам нужно разложить формулу и проследить, какие ионы в ней присутствуют.
Итак, у нас есть два атома хрома (Cr), что указывает на то, что его степень окисления составляет +3. Таким образом, каждый атом хрома в Cr2(SO4)3 имеет степень окисления +3.
Кроме того, у нас есть сульфат (SO4) в составе Cr2(SO4)3. В сульфат-ионе сера (S) имеет степень окисления +6, а оксиген (O) имеет степень окисления -2. Таким образом, чтобы сульфат-ион имел общий заряд -2, атом серы +6 и четыре атома кислорода (-2 * 4 = -8). Сумма этих зарядов равна -2, что является общим зарядом сульфата.
В итоге, соединение Cr2(SO4)3 состоит из двух атомов хрома со степенью окисления +3 и трех сульфатных ионов с общим зарядом -2.
Это интересное соединение обладает рядом полезных свойств и может быть использовано в различных областях, таких как химическая промышленность, лабораторные исследования и технологические процессы.
Разложив химический состав Cr2(SO4)3 на составляющие ионы, мы можем лучше понять его свойства и поведение в различных условиях. Это позволяет нам использовать его эффективно и получать от него максимальную пользу.
Раздел 4. Практическое применение и советы
В данном разделе мы рассмотрели основные способы определения степени окисления хрома и применили их на примере соединения Cr2SO43. Но какие полезные действия и советы можно вынести из этого?
1. Используйте метод периодной системы
Один из самых простых способов определить степень окисления хрома в соединении — использовать метод периодной системы. Этот метод позволяет быстро определить степень окисления хрома, основываясь на его расположении в таблице Менделеева.
2. Учитывайте суммарный заряд соединения
При определении степени окисления хрома необходимо учитывать суммарный заряд соединения. Для этого можно использовать известные заряды других элементов в соединении и вычислить заряд хрома, основываясь на общем заряде соединения.
3. Обратите внимание на окружающую среду
При определении степени окисления хрома необходимо также учитывать окружающую среду и условия реакции. Некоторые соединения могут иметь различные степени окисления в разных условиях, поэтому важно быть внимательным и анализировать все факторы, которые могут влиять на степень окисления хрома.
Используя эти полезные действия и советы, вы сможете более точно определить степень окисления хрома и успешно применить их на практике.






