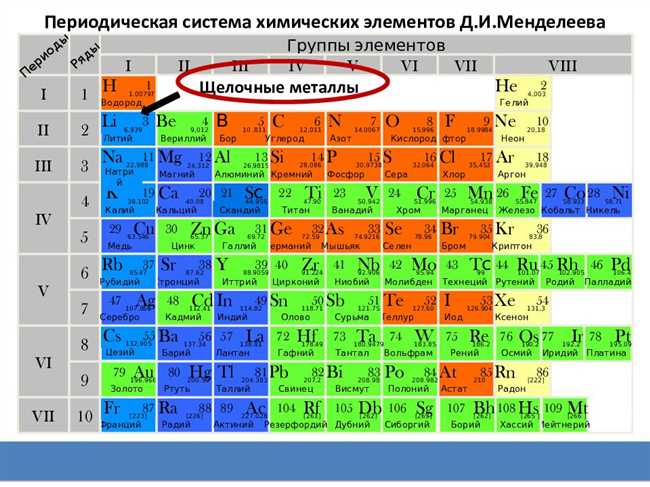
Металлы 1-й группы, также известные как щелочные металлы, включают такие элементы, как литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они характеризуются низкой плотностью, мягкостью и ярко-желтым цветом. Все они являются очень реактивными и легко образуют ионы с положительным зарядом. Эти металлы относятся к первой группе периодической системы элементов и имеют одну внешнюю электронную оболочку, содержащую один электрон. Их химические свойства, такие как способность образовывать сильные щелочные растворы и реагировать с кислородом и водой, делают их полезными в различных сферах, включая производство батарей, лекарственных препаратов и пламени в фейерверках.
Металлы 1-й группы
Щелочные металлы имеют металлический блеск и мягкую, пластичную консистенцию, что делает их легкими для обработки и использования. Они также очень реактивны и образуют ион с положительным зарядом, когда вступают в химические реакции. Эти ионы, известные как катионы, играют важную роль в обеспечении химической активности и металлических свойств элементов 1-й группы.
- Литий (Li): Литий является самым легким металлом и одним из наиболее реактивных элементов 1-й группы. Он играет важную роль в производстве легких и прочных батарей, которые широко используются в электронике и электромобилях.
- Натрий (Na): Натрий является наиболее распространенным щелочным металлом и широко используется в пищевой промышленности для консервирования и приправляния пищи. Он также используется в производстве стекла и мыла.
- Калий (K): Калий является необходимым элементом для растений и используется в сельском хозяйстве в виде удобрений. Он также важен для поддержания здоровья человека и играет роль в функции нервной системы и мышц.
- Рубидий (Rb): Рубидий используется в научных исследованиях, в частности, в атомной физике, благодаря его способности взаимодействовать с электромагнитными полями.
- Цезий (Cs): Цезий также используется в научных исследованиях и имеет много применений в электронике и оптоэлектронике, включая создание фоточувствительных элементов и устройств.
- Франций (Fr): Франций является самым редким и наименее стабильным элементом 1-й группы. Его применение ограничено из-за его радиоактивности и короткого срока полураспада.
В целом, металлы 1-й группы являются незаменимыми элементами в нашей жизни и имеют широкий спектр применений в различных отраслях. Они продолжают исследоваться и использоваться в научных исследованиях и инновационных технологиях, чтобы улучшить нашу жизнь и сделать мир лучше и удобнее. А какой из металлов 1-й группы вам больше всего интересен и почему?
Литий (Li)
Литий является наиболее легким металлом и самым легким металлом из всех элементов, находящихся в периодической таблице. Его низкая плотность делает его идеальным для использования в различных областях.
Литий обладает рядом уникальных свойств, которые делают его ценным материалом. Во-первых, этот металл обладает высокой электроотрицательностью, что делает его хорошим элементом для изготовления литиевых батарей, которые широко применяются в электронике.
Кроме того, литий обладает отличными свойствами термической и электрической проводимости, что делает его полезным материалом для использования в различных системах и технологиях.
Литий также является необходимым элементом для производства прозрачных оксидов, используемых в солнечных батареях и других источниках альтернативной энергии. Этот металл также используется в производстве легких сплавов, которые находят применение в авиации и автомобильной промышленности.
Один из самых интересных аспектов лития – его способность снижать риски случаев самоубийств и биполярного расстройства. Литий считается эффективным препаратом для лечения этих психических заболеваний и его употребление контролируется медицинскими специалистами.
Наш организм каждый день взаимодействует с литием, так как он присутствует в минеральных водах, почве и некоторых продуктах питания. Но не пугайтесь, литий в невредных количествах!
Свойства лития:
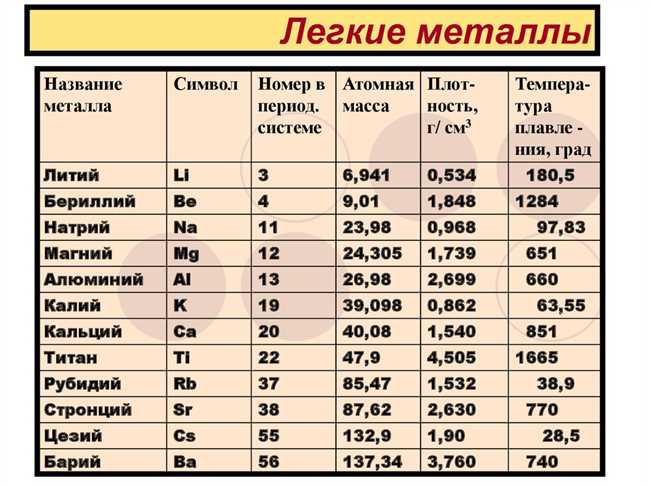
1. Легкий и малореактивный: литий принадлежит к группе легких металлов и является наименее плотным из всех металлов. Он также обладает низкой плавкой и кипятильной температурой. Благодаря этим свойствам, литий широко используется в производстве легких и прочных материалов, в том числе в авиационной и космической промышленности.
2. Огнестойкий и хорошо проводящий тепло: литий обладает высоким теплопроводностью, что делает его полезным материалом для создания теплоотводов в электронике и промышленных процессах.
3. Химически активный: литий реагирует с водой, образуя летучий газ, который может быть использован в качестве топлива. Это свойство делает литий ценным для разработки новых источников энергии, таких как литий-ионные аккумуляторы.
4. Высокая способность к аллотропии: литий может образовывать различные аллотропные модификации (структурные формы), что позволяет ему быть использованным в разных областях, от фармацевтики до пиротехники.
5. Биологически активный: литий имеет важное значение для здоровья человека. Небольшие дозы лития могут быть полезны для лечения психических расстройств, таких как биполярное аффективное расстройство.
- Легкий и малореактивный
- Огнестойкий и хорошо проводящий тепло
- Химически активный
- Высокая способность к аллотропии
- Биологически активный
Видно, что литий обладает широким спектром свойств, которые делают его уникальным и полезным материалом для многих отраслей. И это только некоторые из его множества свойств! Как вы думаете, в каких других областях можно использовать литий?
Применение лития
- Аккумуляторы:
- Лекарственная промышленность:
- Аэрокосмическая промышленность:
- Строительство:
- Железнодорожная промышленность:
Литиевые ионные аккумуляторы широко используются в мобильных устройствах, таких как смартфоны, ноутбуки и планшеты, а также в электромобилях. Они обладают высокой энергетической плотностью, малым весом и длительным сроком службы, что делает их идеальным выбором для портативных устройств.
Литий используется в производстве препаратов, используемых для лечения психических расстройств, таких как биполярное расстройство. Он помогает стабилизировать настроение пациентов и снижает риск рецидивов.
Благодаря своей легкости и высокой коррозионной стойкости, литий используется в производстве компонентов для космических аппаратов и спутников.
Литий добавляется в бетон, чтобы улучшить его прочность и стойкость к агрессивным средам. Это особенно важно в строительстве мостов, дамб и других сооружений, которые должны выдерживать экстремальные нагрузки.
Литий используется в качестве смазочного вещества для улучшения трения и снижения износа между механизмами железнодорожных подвижных составов. Это повышает эффективность работы и продлевает срок службы оборудования.
Это только некоторые примеры применения лития. Этот металл продолжает находить новые области применения и играть важную роль в нашей современной жизни. Как вы считаете, будут ли ещё новые способы использования лития в будущем?
Натрий (Na)
Причина, по которой натрий относится к 1-й группе, заключается в его электронной конфигурации. У атома натрия есть один электрон в своем внешнем энергетическом уровне, что делает его алкалием. Алкалии — это металлы, которые обладают общими свойствами, такими как низкая плотность, мягкость и способность реагировать с водой.
Натрий является очень важным элементом в нашей жизни. Он широко используется в производстве различных материалов, включая стекло, мыло и металлургию. Он также является неизбежным компонентом нашей диеты, поскольку является неотъемлемой частью соли, которую мы употребляем в пищу.
Интересно, что натрий имеет яркую желтую окраску и быстро реагирует с воздухом и водой. По этой причине его хранят под слоем минерального масла или аргонной среды, чтобы предотвратить окисление.
Свойства натрия
1. Атомные свойства
Атомный номер натрия составляет 11. Это означает, что у него 11 электронов и 11 протонов. Натрий имеет 3 электрона на внешнем энергетическом уровне, что делает его склонным к образованию ионов с положительным зарядом.
2. Химические свойства
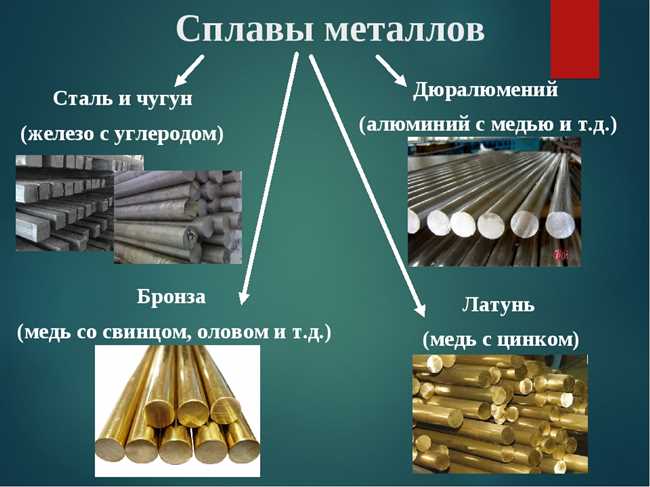
Натрий является очень реактивным металлом и легко реагирует с кислородом воздуха, образуя окислы натрия. Он также реагирует с водой, выделяя водород и образуя щелочь. Это свойство делает его полезным в промышленности и в быту.
- Натрий используется в производстве щелочей, стекол, мыла и ряда других химических продуктов.
- Он также широко применяется в пищевой промышленности в качестве добавки и регулятора pH.
- В медицине натрий используется в качестве компонента инфузионных растворов для восстановления водно-электролитного баланса в организме.
3. Физические свойства
Натрий — мягкий металл, который можно нарезать ножом. Он имеет серебристо-белый цвет и обладает относительно низкой плотностью. Температура плавления натрия составляет около 98 градусов Цельсия, а точка кипения — около 883 градусов Цельсия.
4. Биологические свойства
Натрий является необходимым микроэлементом для нормального функционирования организма. Он участвует в осуществлении нервных импульсов, регулирует баланс воды и многие другие функции. Натрий также находится во многих пищевых продуктах, включая соль.
Заключение: Применение натрия
Одним из основных применений натрия является производство соды. Сода является одним из самых важных химических соединений и используется в таких отраслях, как стекловарение, мыловарение и пищевая промышленность. Натрий также используется в производстве щелочных батарей, которые незаменимы во многих электрических устройствах.
Натрий имеет также широкое применение в медицине. Натрий и его соединения используются для регулирования уровня жидкости в организме, поддержания кислотно-щелочного баланса и выполнения других важных функций. Он также используется в производстве некоторых медицинских препаратов.
Благодаря своей высокой реактивности, натрий находит применение в химической промышленности. Он используется в процессах синтеза органических соединений, получения сплавов с другими металлами и в ряде других химических реакций.
Также натрий используется в ядерной энергетике. Натриевые охладители используются в реакторах для удаления избыточного тепла и защиты от аварийных ситуаций.
В целом, натрий является неотъемлемым элементом многих отраслей и имеет широкий спектр применений. Его химические свойства и доступность делают его важным ресурсом для нашей современной жизни.






