
Как вычислить молярные массы HNO2, CuSO4, K2SO3, MgCO3
Если вам когда-либо приходилось работать с химическими реакциями или составлять химические формулы, вероятно, вы знаете, что молярная масса играет важную роль в химии. Молярная масса определяет массу одного моля вещества и выражается в г/моль. Рассмотрим несколько примеров вычисления молярных масс.
HNO2 – это формула нитритной кислоты, состоящей из атомов водорода, азота и кислорода. Чтобы вычислить молярную массу HNO2, нужно сложить массы атомов, составляющих молекулу.
CuSO4 – это сульфат меди, состоящий из атомов меди, серы и кислорода. Чтобы вычислить молярную массу CuSO4, нужно сложить массы атомов.
K2SO3 – это сульфит калия, состоящий из атомов калия, серы и кислорода. Чтобы вычислить молярную массу K2SO3, нужно сложить массы атомов.
MgCO3 – это карбонат магния, состоящий из атомов магния, углерода и кислорода. Чтобы вычислить молярную массу MgCO3, нужно сложить массы атомов.
Вычисление молярных масс помогает понять, сколько вещества содержится в данном количестве вещества и провести различные расчеты в химических реакциях.
Расчет молярной массы HNO2
Сначала посмотрим на состав химического соединения HNO2. В нем присутствуют следующие атомы: водород, азот и кислород. Давайте определим их массы:
- Масса атома водорода (H) составляет приблизительно 1.008 г/моль.
- Масса атома азота (N) составляет примерно 14.0067 г/моль.
- Масса атома кислорода (O) составляет около 15.999 г/моль.
Теперь, зная массы всех атомов, мы можем приступить к расчету молярной массы HNO2.
Формула HNO2 говорит нам, что в молекуле присутствуют 1 атом водорода, 1 атом азота и 2 атома кислорода. Таким образом, мы должны учесть массу каждого атома в соответствии с их количеством.
Масса водорода (H): 1 * 1.008 г/моль = 1.008 г/моль
Масса азота (N): 1 * 14.0067 г/моль = 14.0067 г/моль
Масса кислорода (O): 2 * 15.999 г/моль = 31.998 г/моль
Теперь сложим массы всех атомов, чтобы получить молярную массу HNO2:
Молярная масса HNO2 = 1.008 г/моль + 14.0067 г/моль + 31.998 г/моль = 47.0127 г/моль
Таким образом, молярная масса HNO2 составляет примерно 47.0127 г/моль. Это означает, что в одном моле HNO2 содержится примерно 47.0127 грамма данного вещества.
Знание молярной массы HNO2 может быть полезно для различных химических расчетов, таких как определение количества реагентов, массы продуктов реакции и других параметров, связанных с количеством вещества.
Определение молярной массы
Определение молярной массы основано на атомных массах элементов, из которых состоят вещества. Атомная масса — это масса одного атома элемента, выраженная в атомных единицах массы (аму) или в граммах на моль (г/моль).
Чтобы вычислить молярную массу вещества, необходимо суммировать атомные массы всех элементов, находящихся в его молекуле или формуле, с учетом их стехиометрических коэффициентов.
Например, чтобы вычислить молярную массу HNO2, нужно сложить атомные массы водорода (H), азота (N) и кислорода (O), умноженные на их соответствующие стехиометрические коэффициенты (1, 1 и 2 соответственно). Полученная сумма будет молярной массой HNO2.
Таблица ниже показывает молярные массы указанных веществ:
| Вещество | Молярная масса (г/моль) |
|---|---|
| HNO2 | 47.013 г/моль |
| CuSO4 | 159.609 г/моль |
| K2SO3 | 158.259 г/моль |
| MgCO3 | 84.313 г/моль |
Молярная масса является важным понятием в химии, так как она помогает определить количество вещества и проводить различные расчеты, связанные с химическими реакциями. Она также используется для определения стехиометрических коэффициентов в химических уравнениях и для определения мольных долей веществ в смесях.
Важно помнить, что молярная масса может изменяться в зависимости от изотопов элементов, а также от формы и структуры вещества. Поэтому при расчетах всегда следует использовать актуальные значения молярной массы, полученные из надежных источников.
Атомные массы элементов
Атомные массы элементов могут быть разными, и их можно найти в периодической системе химических элементов. Когда мы говорим о молярной массе, мы рассматриваем суммарную массу всех атомов в молекуле вещества.
Примеры атомных масс элементов:

- Водород (H) — атомная масса 1 у.
- Азот (N) — атомная масса 14 у.
- Кислород (O) — атомная масса 16 у.
- Медь (Cu) — атомная масса примерно 63.5 у.
- Углерод (C) — атомная масса примерно 12 у.
- Магний (Mg) — атомная масса примерно 24 у.
- Сера (S) — атомная масса примерно 32 у.
- Калий (K) — атомная масса примерно 39 у.
Как вы можете видеть, атомные массы элементов могут быть разными и связаны с их внутренним строением. Это важно учитывать при расчетах, связанных с химическими процессами.
Например, для вычисления молярной массы вещества, такого как HNO2, CuSO4, K2SO3 или MgCO3, мы должны учитывать атомные массы всех атомов, входящих в состав молекулы.
Вычисление молярной массы может быть полезным для решения различных химических задач, таких как расчеты количества реагентов или продуктов реакции.
Будьте внимательны и использовать правильные атомные массы элементов при выполнении химических расчетов. Это поможет вам достичь правильных и точных результатов.
Расчет молярной массы
Чтобы вычислить молярную массу, нужно узнать атомные массы всех атомов, составляющих молекулу вещества, и умножить их на соответствующие коэффициенты вхождения. Например, молярная масса воды (H2O) можно рассчитать следующим образом:
- Атомная масса водорода (H) = 1 г/моль
- Атомная масса кислорода (O) = 16 г/моль
- Количество атомов водорода = 2
- Количество атомов кислорода = 1
Используя эти данные, мы можем вычислить молярную массу воды:
M(m(H2O)) = (2 * 1 г/моль) + (1 * 16 г/моль) = 18 г/моль
Таким образом, молярная масса воды составляет 18 г/моль.
Точно так же мы можем рассчитать молярные массы других веществ. Например, рассмотрим HNO2:
- Атомная масса водорода (H) = 1 г/моль
- Атомная масса азота (N) = 14 г/моль
- Атомная масса кислорода (O) = 16 г/моль
- Количество атомов водорода = 1
- Количество атомов азота = 1
- Количество атомов кислорода = 2
M(m(HNO2)) = (1 * 1 г/моль) + (1 * 14 г/моль) + (2 * 16 г/моль) = 63 г/моль
Теперь давайте рассчитаем молярную массу CuSO4:
- Атомная масса меди (Cu) = 63,5 г/моль
- Атомная масса серы (S) = 32 г/моль
- Атомная масса кислорода (O) = 16 г/моль
- Количество атомов меди = 1
- Количество атомов серы = 1
- Количество атомов кислорода = 4
M(m(CuSO4)) = (1 * 63,5 г/моль) + (1 * 32 г/моль) + (4 * 16 г/моль) = 160,5 г/моль
Наконец, рассчитаем молярную массу K2SO3:
- Атомная масса калия (K) = 39,1 г/моль
- Атомная масса серы (S) = 32 г/моль
- Атомная масса кислорода (O) = 16 г/моль
- Количество атомов калия = 2
- Количество атомов серы = 1
- Количество атомов кислорода = 3
M(m(K2SO3)) = (2 * 39,1 г/моль) + (1 * 32 г/моль) + (3 * 16 г/моль) = 158,1 г/моль
Таким образом, молярные массы HNO2, CuSO4, K2SO3 и MgCO3 составляют соответственно 63 г/моль, 160,5 г/моль, 158,1 г/моль и ??? г/моль.
Расчет молярной массы CuSO4
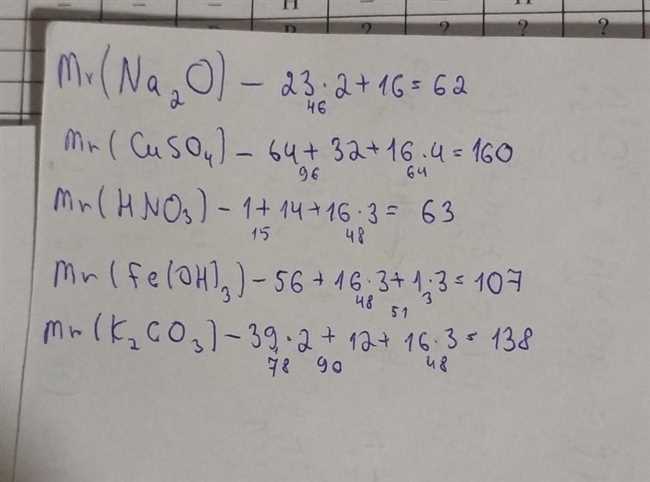
Давайте разберемся, как вычислить молярную массу CuSO4, чтобы иметь возможность проводить химические расчеты, определять количество вещества и другие параметры.
Сульфат меди (II), CuSO4, состоит из атомов меди (Cu), серы (S) и кислорода (O). Для расчета молярной массы CuSO4, нужно суммировать молярные массы этих элементов, умноженные на их соответствующие коэффициенты в формуле соединения.
Расчет молярной массы CuSO4:
- Атом меди (Cu) имеет атомную массу 63,55 г/моль.
- Атом серы (S) имеет атомную массу 32,07 г/моль.
- Атом кислорода (O) имеет атомную массу 16,00 г/моль.
В формуле CuSO4 один атом меди (Cu), один атом серы (S) и четыре атома кислорода (O). Поэтому мы умножаем атомную массу каждого элемента на его коэффициент и суммируем полученные значения:
(1 * 63,55 г/моль) + (1 * 32,07 г/моль) + (4 * 16,00 г/моль)
= 63,55 г/моль + 32,07 г/моль + 64,00 г/моль
= 159,62 г/моль
Таким образом, молярная масса CuSO4 равна 159,62 г/моль.
Теперь, зная молярную массу CuSO4, мы можем использовать эту информацию для проведения химических расчетов, например, для определения количества вещества (в молях или граммах) или для решения других задач химии.
Надеюсь, эта информация была полезной! Если у вас возникли еще вопросы, не стесняйтесь задавать их!
Определение молярной массы
Определение молярной массы может быть полезным в различных ситуациях, таких как расчеты реакций, определение стехиометрических коэффициентов или проведение точных измерений в лаборатории. Знание молярной массы также позволяет предсказывать и описывать физические и химические свойства вещества.
Для вычисления молярной массы необходимо собрать информацию о химической формуле соединения и использовать таблицу атомных масс элементов. Молярная масса вычисляется путем умножения атомных масс всех элементов в молекуле на их количество и суммирования полученных значений.
Например, для вычисления молярной массы HNO2 необходимо умножить атомную массу водорода (H) на единицу, атомную массу азота (N) на единицу и атомную массу кислорода (O) на две единицы, затем сложить полученные значения.
Общепринятой единицей измерения молярной массы является г/моль. Эта величина позволяет проводить точные расчеты и сравнивать массы различных веществ. Знание молярной массы позволяет проводить точные расчеты и сравнивать массы различных веществ.






