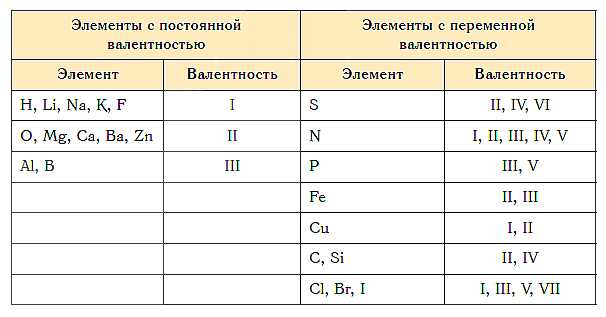
Как определить валентность у C3H8? Почему углерод имеет валентность 4?
Когда речь идет о химических соединениях, одной из важнейших характеристик элементов является их валентность, которая указывает на количество связей, способных образовать атомы данного элемента. Углерод, являющийся главным компонентом органических соединений, обладает валентностью равной четырем. Это означает, что каждый атом углерода может образовать четыре химические связи с другими атомами, включая другие атомы углерода.
Чтобы определить валентность углерода в молекуле C3H8, необходимо учитывать его окружающих атомы и число связей, которые атом углерода образует с ними. В данном случае C3H8 — это молекула пропана, состоящая из трех атомов углерода и восьми атомов водорода. Каждый атом углерода образует по три связи с атомами водорода, и все имеют валентность 4, так как все атомы углерода образуют по четыре химические связи в молекуле.
Таким образом, валентность углерода определяется его способностью образовывать четыре химические связи, что делает его основным элементом в органической химии.
Как определить валентность у C3H8?
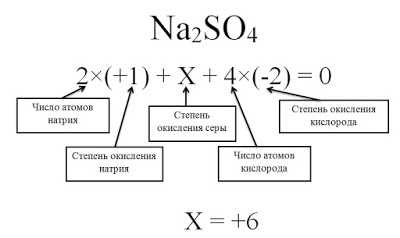
Чтобы определить валентность углерода в молекуле C3H8, необходимо разобраться в его структуре и связях, которые участвуют в образовании этой молекулы.
Структура молекулы C3H8
Молекула пропана (C3H8) состоит из трех атомов углерода (C) и восьми атомов водорода (H). В центре молекулы находится цепочка из трех атомов углерода, причем каждый атом углерода соединен с другими атомами углерода и атомами водорода.
Эта молекула имеет строение алкана, что означает, что все углеродные атомы в ней образуют одинарные связи с другими атомами, а атомы водорода присоединены к ним.
Определение валентности углерода в молекуле C3H8
Валентность углерода — это количество связей, которое этот элемент может образовать с другими элементами. Углерод имеет возможность образовывать четыре связи, поэтому его валентность равна 4.
В молекуле C3H8 каждый атом углерода образует четыре связи: три связи с атомами углерода и одну связь с атомом водорода.
- Первый атом углерода соединен с двумя другими атомами углерода и двумя атомами водорода.
- Второй атом углерода соединен с двумя другими атомами углерода и двумя атомами водорода.
Таким образом, каждый атом углерода в молекуле C3H8 образует по четыре связи, что соответствует его валентности, равной 4.
Итак, валентность углерода в молекуле C3H8 равна 4.
Если у вас остались вопросы по определению валентности углерода в молекуле C3H8 или по другим химическим вопросам, не стесняйтесь задать их в комментариях.
Почему углерод имеет валентность 4

Причина такой валентности углерода кроется в его электронной конфигурации. У углерода есть 4 электрона на его внешнем энергетическом уровне. Эти электроны распределены по четырем орбиталям p. Каждый орбитальный электрон образует связь с другим атомом, обычно другим углеродом или атомом водорода.
Углерод является основным строительным блоком органических молекул, и его способность образовывать 4 химические связи делает его столь важным. За счет своей валентности 4, углерод может образовывать различные типы химических связей и таким образом обеспечивать огромное разнообразие органических соединений.
Например, углерод может образовывать единичные связи с другими углеродами, что приводит к образованию длинных цепей углеродных атомов. Он также может формировать двойные или тройные связи, что позволяет образовывать двойные и тройные связи между атомами углерода и другими атомами.
Кроме того, углерод может образовывать связи с различными элементами, такими как кислород, азот, сера и фосфор, что позволяет ему образовывать разнообразные функциональные группы и создавать сложные органические соединения. Это делает углерод основным элементом в биологии и химической промышленности.
Определение валентности у C3H8
Давайте разберемся с валентностью у молекулы C3H8 или пропана. Валентность указывает на способность атома образовывать связи с другими атомами. Валентность углерода в пропане всегда равна 4.
Химическая формула C3H8 означает, что в молекуле пропана содержатся три атома углерода и восемь атомов водорода. Чтобы определить валентность, нужно знать электронную структуру атомов.
Углерод является элементом группы 14, поэтому у него 4 внешних электрона. Он стремится заполнить или обнести свою внешнюю энергетическую оболочку 8 электронами – это называется октетным правилом.
Основная электронная конфигурация углерода: 1s2 2s2 2p2.
Атом углерода имеет 4 электрона в своей внешней оболочке. Он может поделить 4 своих электрона с 4 атомами водорода, чтобы образовать четыре σ-связи, по одной с каждым атомом водорода. Таким образом, валентность углерода в молекуле пропана равна 4.
Это объясняется тем, что углерод находится во втором периоде, а это значит, что он имеет доступ к 2s и 2p орбиталям, что позволяет углероду формировать четыре связи с другими атомами, чтобы достичь стабильной октетной конфигурации.
Также стоит отметить, что пропан является насыщенным углеводородом, что означает, что в нем все атомы углерода имеют четыре σ-связи и каждый атом водорода имеет одну σ-связь.
Итак, валентность углерода в молекуле C3H8, или пропане, равна 4. Это связано с его электронной структурой и способностью образовывать четыре связи с другими атомами.
Почему углерод имеет валентность 4?
Валентность — это характеристика, которая показывает, сколько электронов может принять, отдать или разделить атом определенного элемента в химической реакции. Углерод имеет валентность 4, потому что у него внешний электронный слой состоит из 4 электронов.
Эти 4 электрона могут образовывать четыре ковалентные связи с другими атомами, что делает углерод очень устойчивым элементом. Такое свойство позволяет углероду формировать разнообразные молекулы, включая органические соединения.
- Углерод имеет валентность 4, так как его внешний электронный слой содержит 4 электрона.
- Это позволяет углероду образовывать четыре ковалентные связи с другими атомами.
- Благодаря своей валентности 4, углерод может образовывать множество различных соединений, что играет важную роль в органической химии.
Именно валентность 4 делает углерод основным строительным блоком многих органических соединений и важным элементом для жизни на Земле.






