- Общая характеристика металлов
- Физические свойства
- Химические свойства
- Роль металлов в нашей жизни
- Типы металлов в периодической системе
- Щелочные металлы
- Щелочноземельные металлы
- Переходные металлы
- Постпереходные металлы
- Лантаноиды и актиноиды
- Редкоземельные металлы
- Щелочные металлы
- Щелочноземельные металлы
- Переходные металлы
- Постпереходные металлы
- Заключение

Металлы — это элементы, которые обладают рядом характерных свойств: хорошей проводимостью электрического тока и тепла, глянцевым блеском, способностью гибко принимать форму и обладают высокой плотностью. В периодической системе химических элементов около 75% всех элементов относятся к металлам. К этой группе относятся как известные нам железо, алюминий, медь, свинец и цинк, так и ряд других элементов, таких как золото, серебро и платина. Металлы обладают широким спектром применения в различных отраслях промышленности, включая авиацию, строительство, электронику и многое другое. Их свойства и вариативность делают их неотъемлемыми компонентами современного мира.
Общая характеристика металлов
Физические свойства
Одна из основных характеристик металлов — это их способность проводить электричество и тепло. У них также высокая плотность и точка плавления, что означает, что они обычно являются твердыми веществами при комнатной температуре, хотя есть и исключения, такие как ртуть. Металлы обладают металлическим блеском и отражают свет, что делает их привлекательными для использования в украшениях и декоративных изделиях.
Один из самых интересных физических свойств металлов — это их способность быть подверженными деформации и переработке. Металлы можно прокатывать, ковать и лить, что делает их идеальными для производства различных изделий и инженерных конструкций.
Химические свойства
Металлы обычно имеют способность образовывать положительные ионы (катионы) благодаря своей низкой электроотрицательности. Они реагируют с кислородом, образуя оксиды, которые впоследствии могут превратиться в растворимые или не растворимые соли в воде.
- Металлы реагируют с кислородом, чтобы образовать оксиды, такие как оксид железа, оксид кальция и оксид магния.
- Некоторые металлы, такие как железо и алюминий, могут реагировать с водой, образуя гидроксиды.
- Металлы также реагируют с кислотами, образуя соли и высвобождая водород.
Металлы обычно имеют высокую реакционную активность, особенно алкалий и щелочноземельные металлы. Они, как правило, более подвержены окислению и коррозии, поэтому требуют специального ухода и защиты.
Роль металлов в нашей жизни
Металлы играют важную роль в нашей повседневной жизни. Они применяются в различных отраслях, таких как строительство, авиация, медицина и энергетика. Металлы широко используются для производства автомобилей, электроники, бытовых приборов и многих других предметов, которые облегчают нашу жизнь и делают ее более комфортной.
Так что в следующий раз, когда вы увидите металлический предмет, задумайтесь о его физических и химических свойствах, а также о том, как он способствует нашему благополучию и прогрессу.
Типы металлов в периодической системе
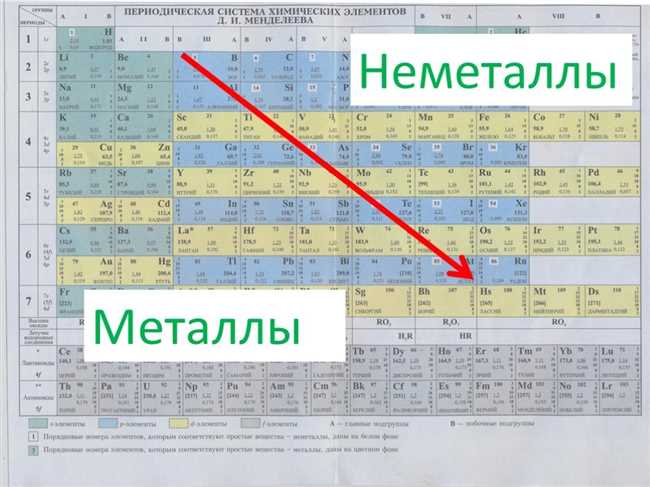
Щелочные металлы
Щелочные металлы — это группа элементов, которые находятся в первой колонке периодической системы. Это литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Щелочные металлы характеризуются высокой реактивностью и низкой плотностью. Они образуют стабильные ионные соединения и обладают высокой проводимостью электричества и тепла. Кроме того, они обладают мягкостью и низкой температурой плавления.
Щелочноземельные металлы
Щелочноземельные металлы — это группа элементов, которые находятся во второй колонке периодической системы. Это бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Щелочноземельные металлы имеют некоторые сходства с щелочными металлами, но они менее реактивны. Они образуют двухзарядные катионы и обладают высокой плотностью и температурой плавления.
Переходные металлы
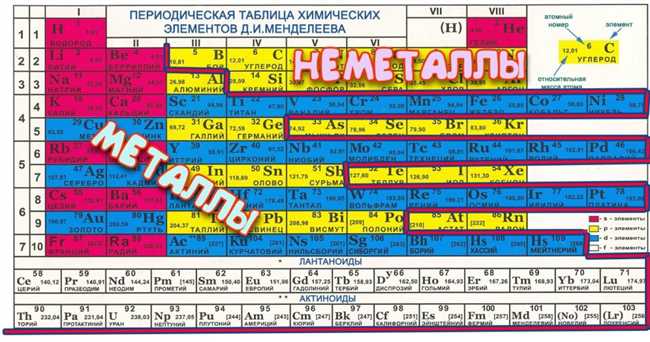
Переходные металлы — это большая группа элементов, которые находятся в середине периодической системы, от скандия (Sc) до лавренция (Lr). Эти элементы обладают разнообразными свойствами и могут образовывать разнообразные соединения. Они являются хорошими проводниками электричества и тепла, обладают высокой плотностью и твердостью. Переходные металлы также играют важную роль в катализаторах и в различных промышленных процессах.
Постпереходные металлы
Постпереходные металлы — это группа элементов, которые находятся между переходными металлами и металлоидами. Они включают элементы от галлия (Ga) до иттрия (Y) и от индия (In) до польния (Po). Постпереходные металлы обладают промежуточными свойствами между металлами и неметаллами. Некоторые из них, такие как индий и олово, имеют низкую температуру плавления и приятный блеск, что делает их полезными в промышленности.
Лантаноиды и актиноиды
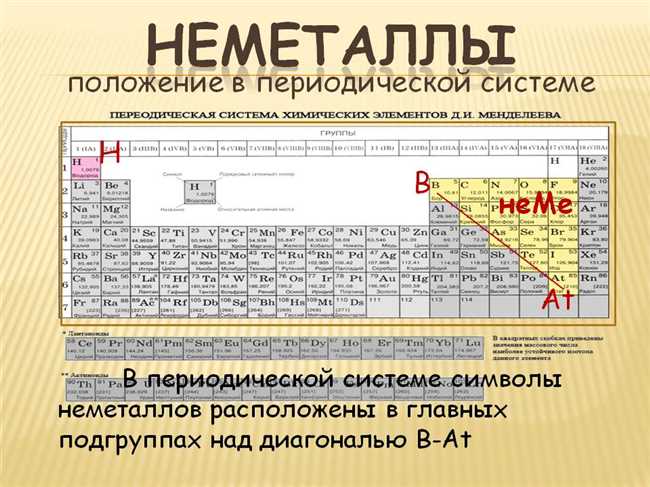
Лантаноиды и актиноиды — это две группы элементов, которые находятся в нижней части периодической системы. Лантаноиды — это элементы от лантана (La) до лютеция (Lu), а актиноиды — это элементы от актиния (Ac) до лоуренция (Lr). Эти элементы обладают сходными свойствами и образуют серии элементов, которые имеют похожую электронную конфигурацию. Лантаноиды и актиноиды имеют разнообразные применения, включая использование в катодах аккумуляторов, ядерной энергетике и медицинских исследованиях.
Редкоземельные металлы
Редкоземельные металлы — это подгруппа лантаноидов и актиноидов, которые обладают особыми свойствами, такими как радиоактивность и магнитные свойства. Они широко используются в производстве магнитов, ламп накаливания, лазерных приборов и других технологических устройствах.
В заключении, периодическая система элементов содержит различные типы металлов, каждый из которых имеет свои уникальные химические и физические свойства. Понимание этих свойств позволяет нам использовать металлы во многих аспектах нашей жизни и развивать новые технологии, которые делают нашу жизнь лучше и комфортнее.
Щелочные металлы
Группа щелочных металлов включает в себя литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Эти элементы имеют общую химическую характеристику — они легко отдают один электрон, образуя положительный ион.
Самым легким щелочным металлом является литий. Он имеет атомный номер 3 и находится в группе элементов, которым нужно всего одно электрон, чтобы заполнить свою внешнюю электронную оболочку и достичь стабильности. Литий является мягким и легким металлом, который часто используется в производстве легких сплавов и литиевых батарей.
Натрий и калий также являются важными щелочными металлами. Натрий широко используется в пищевой промышленности, его соли добавляют в пищу для придания вкуса. Калий играет важную роль в регулировании водного баланса и функциональности мышц и нервной системы. Он находится во многих продуктах питания, включая бананы и картофель.
Рубидий, цезий и франций более редкие щелочные металлы. Они имеют более высокую реактивность и менее распространены в природе. Однако они находят применение в некоторых научных исследованиях и технологиях.
Щелочные металлы имеют много полезных свойств. Они являются отличными проводниками электричества и тепла, а также обладают низкой плотностью и плавкими точками. Благодаря этим свойствам они находят применение в различных отраслях, включая электронику, химическую промышленность, энергетику и металлургию.
- Литий (Li)
- Натрий (Na)
- Калий (K)
- Рубидий (Rb)
- Цезий (Cs)
- Франций (Fr)
Щелочноземельные металлы
Первоначально давайте посмотрим на их химическую природу. Щелочноземельные металлы обладают двумя общими характеристиками: они являются мягкими и имеют низкую плотность. Благодаря этим свойствам, они легко реагируют с другими веществами, особенно с кислородом и водой.
Щелочноземельные металлы используются во многих областях нашей жизни. Например, кальций является неотъемлемой частью нашего организма и необходим для строения костей и зубов. Он также используется в промышленности, особенно в производстве стекла.
- Бериллий (Be) — он имеет высокую прочность и используется в производстве легких и прочных сплавов, которые применяются в авиации и космической промышленности.
- Магний (Mg) — его легкость и прочность делают его идеальным материалом для производства автомобилей и легких конструкций.
- Стронций (Sr) — этот элемент используется во флуоресцентных лампах, которые являются энергосберегающими и дают яркий свет.
- Барий (Ba) — его соединения используются в медицине для проведения рентгеновских исследований и диагностики заболеваний.
- Радий (Ra) — самый редкий и радиоактивный металл из всех щелочноземельных металлов. Он был использован в прошлом для изготовления свечей со светящимся эффектом, но из-за его высокой радиоактивности и опасности для здоровья его использование было ограничено.
Переходные металлы
Переходные металлы включают такие элементы, как железо, медь, цинк, никель, кобальт, марганец, хром и многие другие. Они отличаются от других элементов группой «А» тем, что на их внешней электронной оболочке находится несколько электронов. Это делает их особо реактивными и способными к образованию различных соединений.
Одно из ключевых свойств переходных металлов — это их способность образовывать соединения с переменной степенью окисления. Это означает, что они могут образовывать ионы с различным количеством электронов, что в свою очередь позволяет им участвовать во многих химических реакциях и обладать разнообразными свойствами.
Переходные металлы также являются хорошими проводниками электричества и тепла. Например, медь известна своей высокой электропроводностью, что делает ее идеальным материалом для проводов и электрических контактов. Золото и серебро также являются отличными проводниками и широко используются в ювелирной промышленности.
Переходные металлы также обладают высокой прочностью, что делает их идеальными материалами для строительства и производства различных изделий. Например, железо, благодаря своей прочности и устойчивости к коррозии, широко используется в строительстве мостов и зданий. Титан, который является одним из самых прочных элементов, используется в авиационной и космической промышленности.
Помимо этого, переходные металлы играют важную роль в биологии и медицине. Например, железо является необходимым элементом для синтеза гемоглобина в крови, который отвечает за перенос кислорода в организме. Кобальт используется в производстве витамина В12, который является важным для функционирования нервной системы.
Постпереходные металлы
Однако среди металлов есть такая группа, которая отличается от остальных и называется постпереходными металлами. Постпереходные металлы занимают промежуточное положение между переходными металлами и полупроводниками. Они находятся в периодической системе элементов между группами переходных металлов и неметаллов.
Постпереходные металлы обладают некоторыми сходными свойствами с переходными металлами, такими как блеск и способность образовывать ионы с разными степенями окисления. Но они также проявляют свойства, характерные для неметаллов, например, образование ковалентных связей.
В периодической системе элементов постпереходные металлы включают элементы таких групп, как алюминий (Al), галлий (Ga), индий (In), олово (Sn) и свинец (Pb). Эти элементы имеют широкий спектр применений в различных отраслях, от машиностроения и электроники до химической промышленности и строительства.
Некоторые известные соединения постпереходных металлов, такие как оксиды, сульфиды и галогениды, имеют применения в производстве керамики, стекла, аккумуляторов и других материалов. Благодаря своим свойствам постпереходные металлы являются важными строительными блоками для различных производств и технологий.
Итак, постпереходные металлы — это группа элементов, которая занимает посредственное положение между переходными металлами и неметаллами в периодической системе элементов. Они объединяют в себе свойства и переходных металлов и неметаллов, и имеют широкий спектр применений в различных отраслях промышленности.
Заключение
Все лантаноиды и актиноиды являются радиоактивными, но только некоторые из них являются стабильными изотопами. Эти элементы имеют широкий спектр применений в науке и промышленности. Например, некоторые лантаноиды используются в производстве постоянных магнитов, катализаторов и ламп накаливания. Актиноиды же находят применение в ядерной энергетике, производстве ядерных топливных элементов и в исследованиях квантовой физики.
В целом, лантаноиды и актиноиды являются важными элементами периодической системы, которые отличаются своими уникальными свойствами и применениями. Изучение этих элементов имеет большое значение для развития науки и технологий в различных областях человеческой деятельности.






