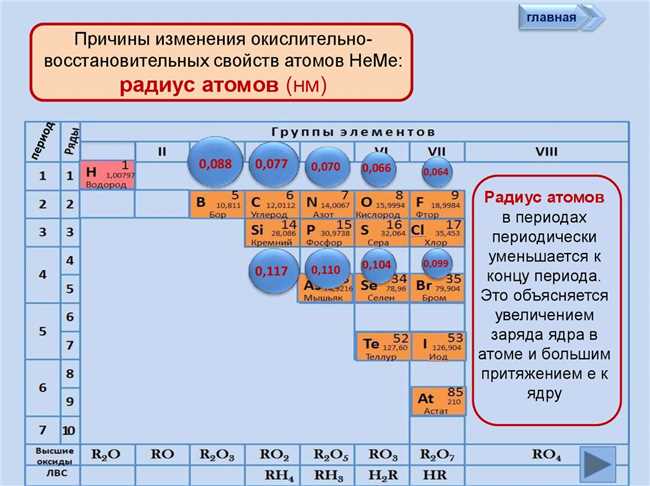
Изучение свойств элементов в периоде и группе таблицы химических элементов позволяет нам понять, какие изменения происходят в химических свойствах металлов и неметаллов.
В периоде, химические свойства элементов изменяются в зависимости от количества энергетических оболочек, атомного радиуса и электроотрицательности. Например, при движении по периоду крайней правой стороны таблицы, металлы становятся менее реактивными и имеют меньший срок службы.
В группе, химические свойства элементов связаны с количеством электронов на внешней оболочке. Металлы, находящиеся на левой стороне таблицы, имеют малое количество электронов на внешней оболочке, что делает их хорошими проводниками электричества и тепла. Неметаллы, находящиеся на правой стороне таблицы, имеют большое количество электронов на внешней оболочке, что делает их плохими проводниками.
Свойства металлов
1. Проводимость и теплопроводность
Металлы обладают высокой проводимостью электричества и тепла. Это объясняется наличием свободных электронов в их кристаллической решетке. Свободные электроны могут двигаться по металлической структуре и передавать электрический ток или тепло. Таким образом, металлы являются отличными материалами для проводников в электрических цепях и теплопереноса.
2. Пластичность и деформируемость
Металлы обладают способностью к пластической деформации. Это значит, что они могут быть легко расплавлены и прокатаны в различные формы без разрушения структуры материала. Благодаря этому свойству, металлы могут быть использованы для создания различных изделий и конструкций. Например, сталь — один из самых популярных металлов, используется в строительстве и производстве автомобилей.
3. Блеск
Металлы обладают блестящей поверхностью. Это связано с тем, что они отражают свет, который падает на их поверхность. Блеск металлов делает их металлы эстетически привлекательными и декоративными. Кроме того, блестящая поверхность металлов также помогает защищать их от коррозии, так как она создает «зеркальные» слои, отражающие внешние воздействия.
4. Износостойкость
Многие металлы обладают высокой износостойкостью, что делает их прочными и долговечными материалами. Износостойкость металлов позволяет им выдерживать механические нагрузки, а также сохранять свои свойства в условиях экстремальных температур и влажности. Благодаря этому свойству, металлы широко используются в производстве механизмов, промышленной техники и других изделий, которые подвержены механическому воздействию.
5. Восстановление

Некоторые металлы обладают способностью к восстановлению после механических или химических повреждений. Это связано с их способностью образовывать оксидные пленки на поверхности, которые защищают металл от дальнейшей коррозии и разрушения. Благодаря этому свойству, многие металлы используются в конструкции кораблей, крыш, автомобилей и других объектов, подверженных агрессивному воздействию окружающей среды.
Надеюсь, теперь вы имеете лучшее представление о свойствах металлов и можете оценить их важность и использование в жизни. Если у вас есть какие-либо вопросы, не стесняйтесь задавать! Я всегда готов вам помочь и поделиться своими знаниями.
Свойства неметаллов
Одним из важных свойств неметаллов является химическая активность. В отличие от металлов, неметаллы часто образуют соединения с металлами, которые обладают металлическими свойствами. Например, неметаллы могут реагировать с металлами, образуя соли. Также неметаллы способны взаимодействовать с другими неметаллами, образуя соединения с характерным неметаллическим химическим свойством.
Неметаллы также обладают способностью к газообразному, жидкому и твердому состоянию. Некоторые неметаллы, как кислород и азот, существуют в газообразном состоянии при нормальных условиях. Другие неметаллы, такие как сера и фосфор, могут существовать в твердом или жидком состоянии. А несколько неметаллов, включая галогены (хлор, бром, йод), могут образовывать вещества, которые при комнатной температуре являются газами или жидкостями.
Однако, несмотря на свою химическую активность и разнообразие состояний, в которых могут находиться неметаллы, они являются важными элементами в нашей жизни. Например, кислород — это неметалл, который играет ключевую роль в жизни всех организмов, так как является необходимым для дыхания. Карбон — еще один неметалл, который является основным строительным материалом органических соединений.
Также стоит отметить, что неметаллы могут обладать различными физическими свойствами. Например, фосфор — это неметалл, который светится синим светом при взаимодействии с кислородом. Забавно, не правда ли?
Изменение свойств в группе
Когда речь заходит о химических элементах и их свойствах, невозможно не упомянуть группы в таблице Менделеева. Группы состоят из элементов, которые имеют общую конфигурацию электронных оболочек, что влияет на их химическое поведение и свойства.
В первую очередь, изменение свойств в группе связано с изменением размера атомов. При движении по группе, размер атомов в целом увеличивается. Это происходит из-за добавления новых электронных оболочек, что приводит к увеличению числа электронов и протонов в атоме. Увеличение размера атомов снижает ионизационную энергию и энергию атомных связей. Это позволяет элементам в группе проявлять более металлические свойства, такие как хорошая проводимость электричества и тепла.
Второй аспект изменения свойств в группе — изменение электроотрицательности. Электроотрицательность — это способность атома притягивать электроны к себе во время химических реакций. В группе элементы, расположенные ближе к верхнему концу, имеют более высокую электроотрицательность. Например, в группе щелочных металлов на первом месте находится литий, который имеет самую низкую электроотрицательность из всех металлов в этой группе. Это связано с тем, что у лития всего одна электронная оболочка, и он готов легко отдать свой электрон, чтобы образовать ион с положительным зарядом. Следующий элемент в группе — натрий — уже имеет две электронные оболочки и более высокую электроотрицательность, но все равно проявляет металлические свойства.
Третий фактор, влияющий на изменение свойств в группе, — количество валентных электронов. Валентные электроны — это электроны на самой последней энергетической оболочке атома. В группе количество валентных электронов увеличивается по мере движения от верхнего конца к нижнему. Это значительно влияет на способность атомов образовывать связи и участвовать в химических реакциях. Например, у газообразного водорода, расположенного в первой группе, есть только один валентный электрон, что позволяет образовывать лишь одну связь с другими атомами во время химических реакций. С другой стороны, у атомов свинца, расположенных в последней группе, семь валентных электронов, что объясняет их способность образовывать связи с другими атомами.
Свойства элементов в группе изменяются из-за различных факторов, таких как размер атомов, электроотрицательность и количество валентных электронов. Это делает изучение групп в таблице Менделеева интересным и захватывающим процессом, который помогает лучше понять химическое поведение различных элементов. Независимо от того, насколько они отдалены друг от друга в таблице, все элементы в группе имеют что-то общее между собой и способны образовывать различные соединения и совершать химические реакции. Такой разнообразный мир элементов заставляет задуматься о чудесах химии и ее влиянии на нашу жизнь, и желание исследовать его дальше.
Заключение

Свойства элементов в периоде меняются по мере увеличения атомного номера. Например, металлические свойства усиливаются при переходе от левой стороны таблицы к правой стороне, так как электроотрицательность элементов увеличивается. Неметаллы, наоборот, обладают более выраженными неметаллическими свойствами с увеличением атомного номера.
Изменение свойств в периоде также проявляется в энергии ионизации и атомном радиусе элементов. С ростом атомного номера энергия ионизации обычно увеличивается, а атомный радиус уменьшается. Это связано с эффективностью защиты электронами в атоме от ядра и сила связи между электронами и ядром.
Таким образом, изменение свойств металлов и неметаллов в периоде является последовательным процессом, отражающим изменение строения атомов и молекул. Периодическая таблица Менделеева помогает систематизировать и описать эти изменения, что позволяет лучше понять химические особенности элементов и их взаимодействия.






