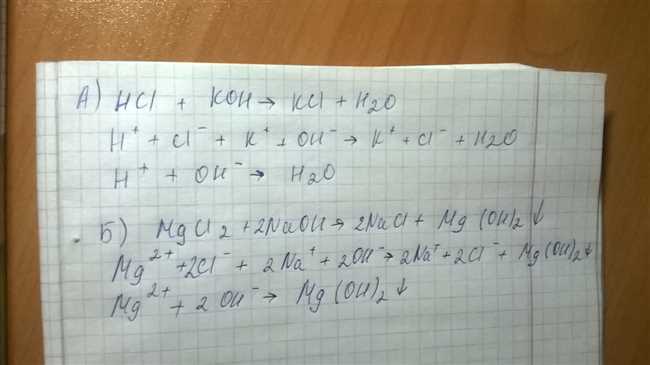
В химии ионные уравнения используются для описания химических реакций, учитывая ионы, образующиеся в процессе. Рассмотрим пример реакции между хлоридом водорода (HCl) и магнием (Mg). Реакция протекает следующим образом:
2HCl + Mg → MgCl2 + H2
В данном случае, две молекулы хлорида водорода (HCl) реагируют с магнием (Mg), образуя хлорид магния (MgCl2) и молекулы водорода (H2).
Ионные уравнения являются удобным способом отображения обмена ионами в веществе, и используются для более полного понимания протекающих химических процессов.
Описание примера
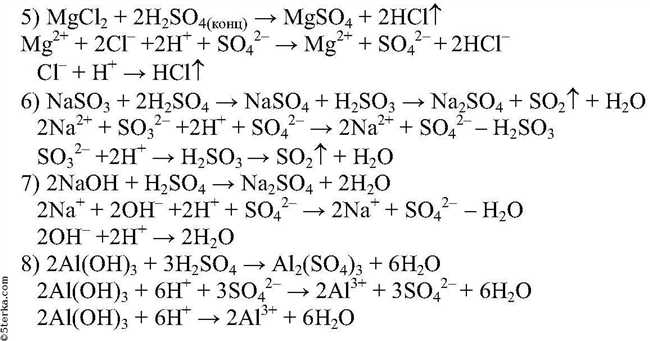
Давайте рассмотрим пример ионного уравнения, которое описывает реакцию между хлороводородом (HCl) и магнием (Mg). Мы хотим узнать, какие вещества образуются при данной реакции и какой ионный состав у этих веществ.
Сначала нужно разложить входящие вещества на ионы. Хлороводород (HCl) разлагается на два иона: ион водорода (H+) и ион хлора (Cl-). Магний (Mg) разлагается на ион магния (Mg2+). Таким образом, ионная формула хлороводорода будет выглядеть так: H+ + Cl- и ионная формула магния будет выглядеть так: Mg2+.
Теперь соберем ионы веществ, которые образуются в результате реакции. Ионы водорода и ионы хлора сопрягаются, образуя молекулы хлороводорода (HCl). Ионы магния и ионы хлора также сопрягаются, образуя молекулы хлорида магния (MgCl2). Таким образом, ионная формула молекулы хлороводорода будет выглядеть так: HCl, а ионная формула молекулы хлорида магния будет выглядеть так: MgCl2.
Кроме того, при данной реакции образуется еще и молекула водорода (H2). Водород образуется благодаря реакции иона водорода (H+) и иона магния (Mg2+), которые сопрягаются и образуют молекулу водорода. Ионная формула молекулы водорода будет выглядеть так: H2.
Таким образом, в результате реакции хлороводорода (HCl) и магния (Mg) образуются следующие вещества: хлороводород (HCl), хлорид магния (MgCl2) и водород (H2).
Надеюсь, данное объяснение помогло вам понять пример ионного уравнения реакции между HCl и Mg и какие вещества образуются при данной реакции.
Уравнение реакции
В данной теме мы рассмотрим уравнение реакции между хлороводородом (HCl) и магнием (Mg), которая приводит к образованию хлорида магния (MgCl) и водорода (H2). Уравнения реакций позволяют описать, какие вещества реагируют и какие продукты образуются при данной реакции.
Давайте начнем с ионной формулы для каждого из веществ:
- Хлороводород (HCl) — состоит из положительного иона водорода (H+) и отрицательного иона хлора (Cl-).
- Магний (Mg) — представляет собой положительный ион магния (Mg2+).
- Хлорид магния (MgCl) — состоит из положительного иона магния (Mg2+) и отрицательного иона хлора (Cl-).
- Водород (H2) — состоит из двух атомов водорода, образующих молекулу.
Теперь мы можем записать уравнение реакции:
HCl + Mg → MgCl + H2
Здесь сначала указаны реагенты — хлороводород и магний, а затем продукты — хлорид магния и водород. Также заметим, что уравнение реакции должно быть сбалансировано, то есть количество атомов каждого элемента должно быть одинаковым на обеих сторонах уравнения. В данном случае уравнение уже сбалансированное.
Это уравнение позволяет описать реакцию, которая происходит между хлороводородом и магнием, и предсказать, какие продукты образуются. Уравнения реакций имеют большое значение в химии, так как они помогают понять и объяснить механизмы реакций и определить состав и свойства образующихся продуктов.
Решение уравнения
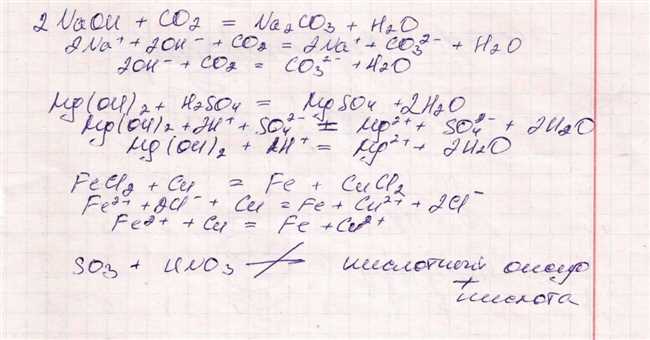
Когда HCl растворяется в воде, он полностью диссоциирует на ионы водорода (H+) и ионы хлорида (Cl-). То есть, HCl становится H+ + Cl-. Оксид магния также может раствориться в воде и диссоциировать на ионы магния (Mg2+) и ионы оксида (O2-). Итак, у нас есть ионные формы обоих веществ: H+ + Cl- и Mg2+ + O2-.
Теперь мы можем рассмотреть реакцию между HCl и Mg. Ионы Cl- и ионы Mg2+ образуют соединение MgCl. Полученная формула будет MgCl2. Таким образом, наше уравнение превращается в H+ + Mg2+ = MgCl2 + H2.
Осталось только проверить сбалансированность уравнения. Если мы посмотрим на количество атомов каждого элемента, то увидим, что с обеих сторон уравнения есть один атом магния, два атома хлора и два атома водорода. Значит, уравнение сбалансировано.
Таким образом, ионное уравнение HCl + Mg = MgCl2 + H2 сбалансировано и описывает реакцию между соляной кислотой и оксидом магния, которая приводит к образованию хлорида магния и водорода.
Объяснение каждого шага
1. Ионизация веществ:
Первым шагом в решении данного ионного уравнения является ионизация исходных веществ — HCL и Mg. В результате ионизации HCL превращается в ионы H+ и Cl-, а Mg в ионы Mg2+.
2. Образование продуктов:
Затем происходит образование продуктов реакции — MgCl и H2. В данном случае ионы H+ соединяются с ионами Cl- и образуют молекулы HCl, а ионы Mg2+ соединяются с молекулами H2 и образуют молекулы MgCl2.
3. Составление ионного уравнения:
Ионное уравнение представляет собой запись реакции с учетом ионов, которые участвуют в реакции. В данном случае ионное уравнение будет выглядеть следующим образом:
- H+ + Cl- + Mg → Mg2+ + Cl- + H2
4. Упрощение ионного уравнения:
В ионном уравнении присутствуют ионы Cl-, которые одновременно являются реагентами и продуктами. Поэтому данные ионы могут быть упрощены, и ионное уравнение примет следующий вид:
- H+ + Mg → Mg2+ + H2
5. Проверка сбалансированности уравнения:
Наконец, необходимо проверить сбалансированность данного уравнения. Для этого нужно убедиться, что количество атомов каждого элемента на обеих сторонах уравнения одинаково. В данном случае уравнение уже сбалансировано, так как количество атомов каждого элемента равно 1 на обеих сторонах уравнения.






