- Щелочь: определение и свойства
- Определение щелочи
- Химический состав щелочи
- Формула щелочи
- Физические свойства щелочи
- 1. Растворимость в воде
- 2. Растворяющая способность
- 3. Вкус и запах
- 4. Гигроскопичность
- 5. Теплопроводность
- 6. Вязкость
- 7. Электропроводность
- 8. Показатель pH
- 9. Вспенивание
- Химические свойства щелочи
- Применение щелочи
- 1. Промышленное применение
- 2. Бытовое применение
Щелочь — это класс химических веществ, которые имеют высокую концентрацию гидроксидов или оксидов металлов. Они обладают рядом особых свойств, которые делают их полезными в различных областях.
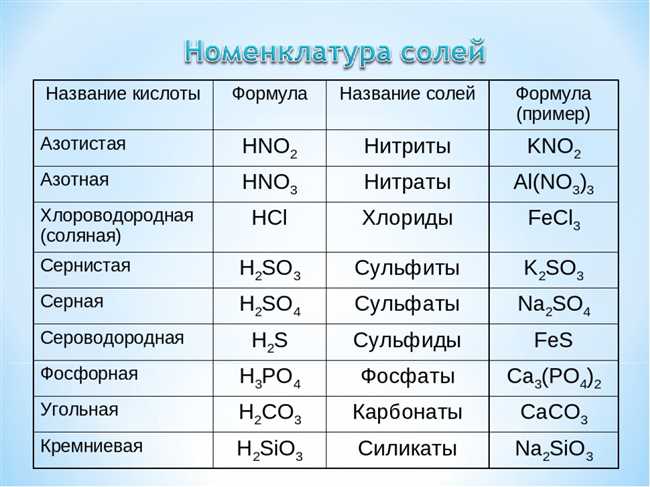
Химическая формула щелочи обычно представляет собой комбинацию символов металла и гидроксидной группы. Наиболее распространенные щелочи включают в себя гидроксид натрия (NaOH) и гидроксид калия (KOH).
Щелочи имеют широкий спектр применений, включая использование в бытовых и промышленных продуктах, как моющие средства, алкалийные батареи, легирование металлов и многое другое. Они также играют важную роль в химической промышленности и процессах очистки воды.
Щелочь: определение и свойства
Одной из самых известных щелочных соединений является гидроксид натрия, также известный как каустическая сода. Его химическая формула — NaOH. Гидроксид натрия представляет собой белые кристаллические гранулы с сильно щелочной реакцией. Этот продукт широко используется в промышленности для производства мыла, стекла и множества других продуктов.
Свойства щелочей включают следующее:
- Щелочи растворяются в воде: образуется гидроксидное ионное соединение.
- Щелочи обладают щелочной реакцией: они изменяют цвет красного лакмусового бумажного индикатора с красного на синий.
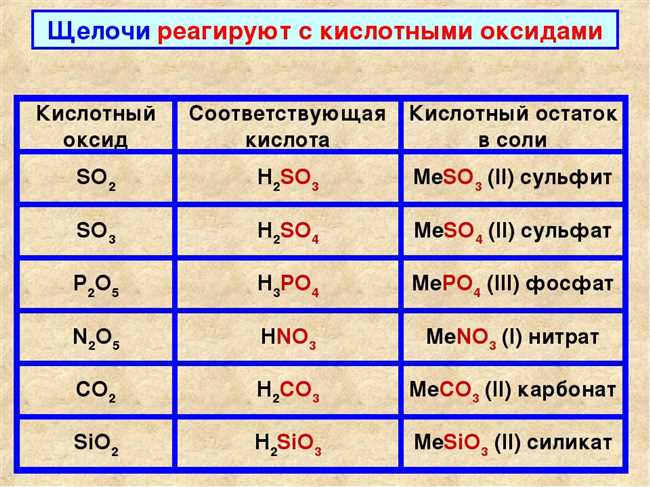
- Щелочи реагируют с кислотами: нейтрализация кислот осуществляется с образованием солей и воды.
- Щелочи имеют высокую щелочную активность: они могут образовывать основания и ионы гидроксила, которые являются катионами с отрицательным зарядом.
- Щелочи имеют высокую плотность энергии: это означает, что они могут быть опасными и должны использоваться с осторожностью.
Щелочи используются в различных отраслях промышленности, включая производство стекла, мыла, моющих средств, шампуней и многих других продуктов. Они также используются в аналитической химии для регулирования pH растворов и в медицине для нейтрализации кислотных ожогов.
Определение щелочи
Щелочи имеют определенный химический состав. Одна из наиболее распространенных и известных щелочей — гидроксид натрия, также известный как каустическая сода или едкая сода. Его химическая формула NaOH. Гидроксид натрия — очень сильное основание и является одним из наиболее распространенных промышленных продуктов, который используется в различных отраслях, таких как производство стекла, мыла и бумаги.
Основные свойства щелочей включают:
- Обладание высоким pH-значением. Щелочи имеют значения pH выше 7, что указывает на их щелочную природу. Чем выше значение pH, тем более щелочным является раствор.
- Образование гидроксидных ионов (OH-) в водном растворе. Гидроксидные ионы имеют основные свойства и могут нейтрализовать кислоты.
- Взаимодействие с кислотами для образования солей и воды. Щелочи могут реагировать с кислотами в реакции нейтрализации, при которой образуются соли и вода.
Помимо гидроксида натрия, щелочи также могут иметь другие химические формулы, такие как гидроксид калия (KOH), гидроксид аммония (NH4OH) и гидроксид кальция (Ca(OH)2). Они также обладают щелочными свойствами и нашли широкое применение в различных отраслях промышленности и повседневной жизни.
Теперь, когда вы знаете, что такое щелочь, вы можете легко определить ее по ее химическому составу и основным свойствам. Не забывайте, что щелочи имеют высокое pH-значение, образуют гидроксидные ионы в водном растворе и могут реагировать с кислотами для образования солей и воды.
Химический состав щелочи
Щелочи состоят из анионов, которые образуются при растворении оснований в воде. Они могут быть представлены различными химическими формулами, но наиболее распространенным и известным представителем щелочей является гидроксид натрия (NaOH). Гидроксид натрия является основным компонентом таких продуктов, как линолеум, стиральные порошки и многие другие.
Также щелочи могут содержать анионы других элементов, например, гидроксид калия (KOH). Гидроксид калия широко используется в лабораторной практике, особенно в качестве щелочной среды.
Интересно отметить, что щелочи обладают высокой растворимостью в воде, что объясняет их широкое применение в различных областях. Когда щелочь растворяется в воде, образуется гидроксидный ион OH-, который отвечает за выраженные основные свойства щелочи. Гидроксидный ион обладает способностью принимать от веществ кислородные и водородные ионы, что позволяет щелочам поддерживать pH-баланс вещества и регулировать его кислотность или щелочность.
Таким образом, химический состав щелочи представлен гидроксидными ионами, которые при растворении в воде образуют щелочные растворы. Эти растворы обладают основными свойствами и широко используются в промышленности и быту. А вы уже знали, что химический состав щелочи? Какие еще удивительные свойства они могут иметь? Поделитесь своими мыслями в комментариях!
Формула щелочи
Общая формула щелочи выглядит следующим образом: MOH, где M — металл, а OH — гидроксильная группа. Гидроксиды щелочных металлов (например, гидроксид натрия, гидроксид калия) являются наиболее распространенными и хорошо известными щелочными соединениями.
Однако следует отметить, что щелочи могут иметь и другие формулы, в зависимости от своего состава. Например, аммиак (NH3) также может рассматриваться как щелочь, хотя его формула отличается от общей формулы щелочи. Аммиак является щелочью, поскольку образует щелочные растворы и обладает щелочными свойствами.
Щелочи обычно обладают рядом характерных свойств, таких как щелочная реакция (т.е. способность нейтрализовать кислоты), образование гидроксидов и способность растворяться в воде. Они также способны образовывать ионы гидроксида (OH-) в растворе, что делает их сильными щелочами.
В конечном итоге, формула щелочи может варьироваться в зависимости от ее состава, но общая формула MOH является характерной для большинства щелочей. Эти соединения имеют важное применение в различных областях, от химической промышленности до бытовых нужд.
Физические свойства щелочи
1. Растворимость в воде

Щелочи весьма растворимы в воде. Это означает, что их молекулы активно взаимодействуют с молекулами воды, образуя гидроксидные ионы. Это свойство делает щелочные растворы отличными для использования в различных областях жизни, таких как промышленность, химия и бытовая сфера.
2. Растворяющая способность
Щелочи обладают высокой растворяющей способностью и могут растворять многие другие вещества. Это важное свойство находит применение в множестве процессов, например, при очистке и обработке различных материалов.
3. Вкус и запах
Щелочные растворы обычно имеют горький вкус и специфический запах. Это свойство делает их легко узнаваемыми и позволяет отличить щелочные растворы от других веществ.
4. Гигроскопичность
Щелочные вещества обладают гигроскопичностью — свойством активно поглощать влагу из окружающей среды. Это объясняет, почему щелочи часто используются для сушки и осушения различных материалов.
5. Теплопроводность
Щелочи, как и многие другие соединения, обладают хорошей теплопроводностью. Они способствуют передаче тепла и могут использоваться в различных теплотехнических приложениях.
6. Вязкость
Некоторые щелочные растворы обладают высокой вязкостью, что означает, что они имеют сравнительно большую течение. Это свойство может быть полезно в разных процессах, например, в производстве жидких моющих средств.
7. Электропроводность
Щелочные растворы являются хорошими проводниками электричества. В них образуются ионы, которые способны перемещаться под воздействием электрического поля. Именно поэтому щелочные растворы используются в электролизе и других электрохимических процессах.
8. Показатель pH
Щелочные растворы часто имеют высокие значения показателя pH, что означает, что они щелочные и имеют щелочную реакцию. Показатель pH позволяет определить кислотность или щелочность раствора и является важным показателем его химических свойств.
9. Вспенивание
Некоторые щелочи способны образовывать вспененные структуры при взаимодействии с воздухом или другими веществами. Это свойство может быть полезным в процессах, связанных с производством пены или шампуней.
Итак, физические свойства щелочи весьма разнообразны и определяют их уникальные химические и физические характеристики. Щелочи имеют широкий спектр применений и играют важную роль в различных отраслях нашей жизни.
Химические свойства щелочи

1. Щелочи обладают способностью нейтрализовывать кислоты.
Одним из главных химических свойств щелочи является их способность нейтрализовывать кислоты. Это происходит в результате реакции между щелочными и кислотными ионами, которая приводит к образованию солей и воды. Например, щелочь натрия (NaOH) и соляная кислота (HCl) реагируют, образуя соль NaCl и воду:
NaOH + HCl → NaCl + H₂O
Именно благодаря этой способности щелочи широко применяются в бытовых условиях для очистки и нейтрализации различных поверхностей и жидкостей.
2. Щелочи отрицательно влияют на кислотную реакцию.
Если вы помните с уроков химии, кислотная реакция характеризуется повышенной концентрацией иона водорода (H⁺). Щелочи же содержат ионы гидроксида (OH⁻). Когда кислота и щелочь взаимодействуют, ионы гидроксида (OH⁻) нейтрализуют ионы водорода (H⁺), и реакция становится более уравновешенной и менее кислой.
3. Щелочи обладают амфотерными свойствами.
Щелочи также могут взаимодействовать с кислотами и проявлять амфотерные свойства. Это значит, что щелочь может действовать как кислота в присутствии более сильной кислоты и как основание в присутствии более слабой кислоты. Например, гидроксид алюминия (Al(OH)₃) может реагировать с кислотой соляной (HCl) и проявлять свои амфотерные свойства:
Al(OH)₃ + HCl → AlCl₃ + H₂O
Это свойство щелочей позволяет им применяться в различных химических процессах и реакциях.
Щелочи обладают рядом уникальных химических свойств, которые позволяют им широко применяться в различных сферах нашей повседневной жизни. Они могут нейтрализовывать кислоты, уравновешивать кислотную реакцию и проявлять амфотерные свойства. Важно помнить, что правильное и безопасное использование щелочей имеет ключевое значение, и всегда следует соблюдать все рекомендации по их применению.
Применение щелочи
Щелочи имеют широкий спектр применения как в промышленности, так и в бытовых условиях. Они используются в различных отраслях, таких как химическая, пищевая, фармацевтическая, металлургическая, текстильная и другие.
1. Промышленное применение
В промышленности щелочи используются для проведения различных химических процессов. Например, щелочи могут быть использованы в производстве бумаги и целлюлозы, переработке нефти и газа, очистке металлов от загрязнений, производстве стекла и прочих материалов.
Также щелочи могут быть использованы в качестве растворителей для удаления различных загрязнений и отложений, а также для устранения накипи и ржавчины.
2. Бытовое применение
Щелочи широко применяются в бытовых условиях. Они являются ключевым компонентом моющих средств, таких как стиральные порошки, моющие гели и жидкости, для удаления пятен и загрязнений с различных поверхностей. Щелочные растворы также используются для очистки сантехники и кухонных поверхностей.
Кроме того, щелочи могут быть использованы в качестве добавки в пищевых продуктах, таких как печенье и жидкости для чистки овощей. Они могут применяться для регулирования pH-уровня, консервирования пищевых продуктов или для улучшения их текстуры и вкуса.
Таким образом, щелочи играют важную роль в различных областях и широко применяются в промышленности и повседневной жизни.






