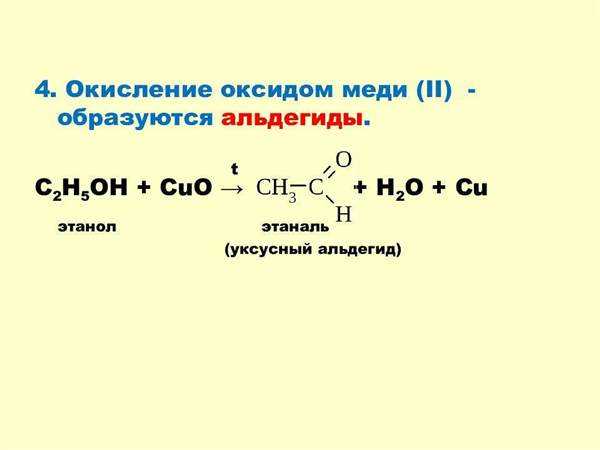
Когда медь окисляется, образуются различные соединения, которые могут иметь разные свойства и цвета. Этот процесс происходит из-за взаимодействия меди с кислородом воздуха или других окислителей. Одним из наиболее известных соединений, образующихся при окислении меди, является медный оксид (Cu2O). Он обладает красно-коричневым цветом и широко используется в производстве красок, керамики, электроники и других отраслях. Также, при окислении меди могут образовываться другие оксиды, такие как медный оксид (CuO) и медный пероксид (CuO2). Каждое из этих соединений имеет свои уникальные свойства и применения. Оксидированная поверхность меди может быть использована, например, для защиты металла от дальнейшей коррозии или как декоративный элемент в различных изделиях.
Образование оксидов меди
Существует несколько оксидов меди, самыми распространенными из которых являются оксид меди(II) (CuO) и оксид меди(I) (Cu2O).
Оксид меди(II) (CuO)
Оксид меди(II) (CuO), также известный как черный оксид меди, образуется при полном окислении меди. Этот оксид имеет чёрный цвет и обладает свойствами полупроводника. Он широко используется в производстве керамики, магнетиков и в других промышленных процессах.
Оксид меди(I) (Cu2O)

Оксид меди(I) (Cu2O), также известный как красный оксид меди, образуется при частичном окислении меди. Этот оксид имеет красновато-коричневый цвет и хорошо растворим в щелочной среде. Okислительные свойства красного оксида меди позволяют ему использоваться в производстве оптических стекол, каталитических веществ и других применениях.
Образование оксидов меди является важным процессом, который происходит в природе и в промышленных процессах. Эти соединения имеют широкий спектр применения и играют важную роль в различных отраслях, включая электронику, керамику, катализ и другие.
Образование солей меди

Когда медь окисляется, она может образовывать различные соли. Это происходит, когда медь взаимодействует с окислителями, такими как кислород или кислоты. Медная соль образуется при окислении меди в присутствии соответствующих реактивов.
Одной из самых известных солей меди является сульфат меди(II) или сернокислая медь. Она образуется, когда медь взаимодействует с серной кислотой. Сернокислая медь имеет синий цвет и широко используется в различных областях, включая химическую промышленность и сельское хозяйство.
Другой распространенной солью меди является хлорид меди(II) или хлористая медь. Он образуется при реакции меди с хлоридной кислотой или хлорным газом. Хлористая медь используется для производства пигментов, керамики и стекла, а также в медицине и электронике.
Еще одной известной солью меди является нитрат меди(II) или азотнокислая медь. Он образуется при реакции меди с азотной кислотой. Азотнокислая медь широко используется в химической промышленности для производства пигментов и красителей.
Кроме того, медь может образовывать другие соли, такие как ацетат меди(II), гидроксид меди(II) и карбонат меди(II). Каждая из этих солей имеет свои уникальные свойства и применения.
- Соль: сернокислая медь (CuSO4)
- Образуется при: реакции меди с серной кислотой
- Используется в: химической промышленности, сельском хозяйстве
- Соль: хлористая медь (CuCl2)
- Образуется при: реакции меди с хлоридной кислотой или хлорным газом
- Используется в: производстве пигментов, керамики, стекла и в медицине
- Соль: азотнокислая медь (Cu(NO3)2)
- Образуется при: реакции меди с азотной кислотой
- Используется в: химической промышленности для производства пигментов и красителей
Таким образом, окисление меди может привести к образованию различных солей, которые имеют широкое применение в различных отраслях промышленности и науки.
Образование гидроксида меди
Гидроксид меди образуется при реакции меди с водой или раствором гидроксида натрия, калия или аммиака. Эта реакция может происходить естественным образом, например, когда медный предмет оставляют на воздухе или погружают в воду.
Гидроксид меди имеет формулу Cu(OH)2. Он является зеленовато-голубым соединением, которое может быть в виде порошка или кристаллов. Гидроксид меди плохо растворим в воде, но легко диссоциирует, освобождая ионы меди и гидроксида.
Образование гидроксида меди можно проиллюстрировать следующей реакцией:
2Cu + 2H2O → Cu(OH)2 + H2
Эта реакция показывает, что две молекулы меди (Cu) реагируют с двумя молекулами воды (H2O), образуя одну молекулу гидроксида меди (Cu(OH)2) и выделяя одну молекулу водорода (H2).
Гидроксид меди используется в различных областях, от химической промышленности до производства косметических средств. Он обладает свойствами, которые делают его полезным в качестве катализатора, пигмента, антисептика и стабилизатора для некоторых материалов.
Таким образом, образование гидроксида меди при окислении меди — это важный процесс, который имеет множество применений в различных сферах науки и промышленности.
Заключение
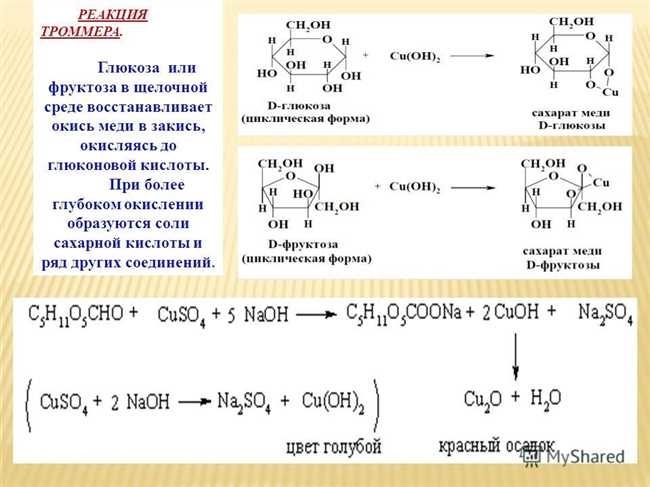
Оксид меди (в основном медный(II) оксид) используется в качестве катализатора, а также в производстве керамики и стекла. Он также используется в переработке полимерных материалов, микроэлектронике и других промышленных процессах.
Соли меди имеют широкое применение в производстве красок, пигментов и косметических продуктов. Они также используются в медицине для создания антибактериальных и антисептических препаратов.
Гидроксид меди широко используется в электротехнике для создания электролитических медных покрытий на поверхности различных материалов. Он также используется в производстве мыла, стекла, лаков и других продуктов.
Применение оксидов, солей и гидроксида меди является неотъемлемой частью современной технологии. Они играют важную роль в производстве различных материалов и продуктов, а также находят применение в медицине, электротехнике и других отраслях науки и промышленности. Открытие новых способов их использования и разработка новых материалов на их основе являются актуальными задачами для дальнейших исследований и развития научно-технического прогресса.






